【云回顾】一图读懂API工艺研究的项目规划和管理
2020年04月09日,美迪西工艺部高级主任罗万荣博士为我们分享了IND阶段API工艺研究的项目计划与管理心得。大家可以点击文末的“观看精彩视频”,进入视频回放链接,观看完整视频!
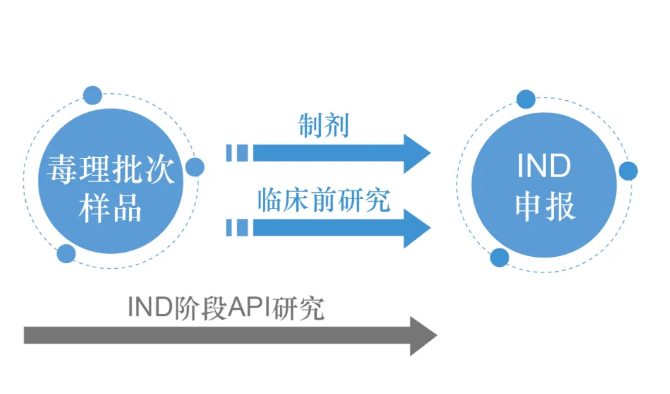
项目规划
需平衡的三大要素
✔质量√效率√成本
批次设计
| 批次设计需要考虑的因素 | 申报类型 | FDA:主要关注毒理、临床批次,可以一个批次;
NMPA:一般三批次,安评,中试,临床批次
多申报:综合考虑 |
| 项目周期 | 申报计划 |
| 制剂需求 | 剂型;剂量 |
| 批量 | 生产规模和批量的关系,取决于毒理数据、临床方案 |
起始物料的选择
| 物料设计需要考虑的因素 | 杂质--可以有效控制 |
| 结构--拥有明确的化学特性和结构;原料药结构片段 |
| 分析方法--开发稳定的分析方法 |
质量控制
杂质研究

✔基因毒性杂质
| GTI(基因毒性杂质) | PGI(潜在基因毒性杂质) |
| 甲磺酸甲酯、氯甲烷、NDMA等严格控制,建议避免出现;如果在生产中用到二X胺类,硝酸亚硝酸类,或生产线、容器、自来水中含有这些物质的,需要特别注意。 | 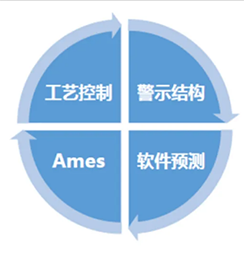 |
✔元素杂质 √ > 0.1%的杂质
质量研究
不需要完整的方法验证,至少包括专属性和灵敏度,鼓励做更多。
稳定性研究
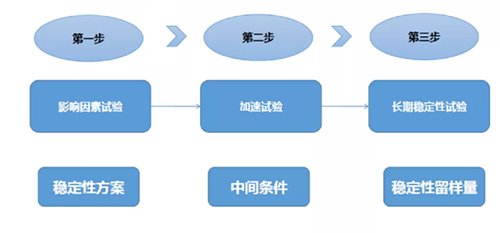
压力试验

美迪西工艺部
~6,000m 2 实验室~150名员工
▲ 专业的API技术平台
▲ 完善的分析测试中心
▲ 微生物实验室
▲ 工艺安全评价实验室
▲ GMP车间和精烘包(D级)
▲ 一站式、系统化的API研发服务
往期精彩回顾
美迪西云讲堂第01讲:
美迪西云讲堂第02讲:
美迪西云讲堂第03讲:
美迪西云讲堂第04讲:
美迪西云讲堂第05讲:
美迪西云讲堂第06讲:
美迪西云讲堂第07讲:
美迪西云讲堂第08讲:
美迪西云讲堂第09讲:
联系我们:
电话: +86 (21) 5859-1500(总机)

分享到:








