截至2025年末,公司已成功助力32个ADC药物获批临床,并有20余个ADC项目正在推进中。美迪西助力的ADC药物研发项目包括:
2021年6月,多禧生物用于治疗晚期实体瘤的1类ADC药物注射用重组人源化抗MUC1单抗-Tub201偶联剂获批临床。美迪西在MUC1新药研发中,提供了包括药效学、药代动力学及安全评价等全套临床前研究服务,助力项目成功获批临床。
2021年12月,多禧生物DXC007项目成功获批临床试验。该药适应症为成年人中最常见的急性白血病——复发/难治急性髓系白血病(AML)。在DXC007的研发中,美迪西提供了包括药代、安全评价及SEND转化服务,助力项目成功获批临床。在安全性评价试验中,美迪西毒理研究部遵循ICH指导原则S6和S9,结合DXC007项目具体情况,定制了个性化安全性评价方案,为其提供符合NMPA、FDA等国际GLP标准的安全性评价服务。
2022年4月,百奥泰注射用BAT8006获批临床,用于治疗晚期实体瘤。该药为靶向叶酸受体α(FRα)的ADC药物。美迪西科研骨干依托成熟的ADC临床前研发服务平台,汲取多年在ADC药物临床前研发领域的实战技术和经验,遵循ICH指导原则S6和S9,结合BAT8006项目的具体情况,为其定制了个性化的安全性评价方案,攻克了药物抗体比(DAR)、稳定性带来的复杂性和多样性等难题,全力保障BAT8006安全性评价试验高效、高质的研发。
2023年3月,轩竹生物及其旗下全资子公司轩竹康明生物KM501获得临床试验批件。KM501是完全敲除岩藻糖的双抗ADC药物,适用于治疗HER2阳性/表达、扩增或突变的局部晚期/转移性实体瘤,包括HER2低表达的相关晚期肿瘤。KM501为靶向HER2两个不同结构域双特异性抗体ADC偶联物。美迪西作为轩竹生物的合作伙伴,为KM501提供了符合GLP规范的临床前研究服务,包括药代动力学研究和安全性评价。
2023年11月,华奥泰收到美国FDA通知,同意公司研发的靶向CD73抗原的第三代ADC项目HB0052进入临床试验。HB0052是基于华奥泰抗体偶联药物平台研发的首款以拓扑异构酶抑制剂为载荷的First-in-Class创新型免疫抑制靶点的ADC,具有双重抗肿瘤机制,在多个实体瘤适应症具有应用潜力。作为华奥泰的合作伙伴,美迪西依托抗体药物偶联物研发服务平台及其专业的技术能力和丰富的项目经验,为HB0052的研发提供了符合GLP规范的药代、安评试验,保障项目高质高效推进。
2023年12月,安谛康自主研发的 “儿童版”抗流感1类新药ADC189颗粒的临床试验申请(IND),获得了中国国家药品监督管理局药品审评中心(CDE)受理。美迪西作为安谛康的合作伙伴,为ADC189提供了的制剂研究服务,助力其快速推进临床前研发进程。
2024年2月,国药集团中国生物上海生物制品研究所自主研发的第二款I类创新型ADC药物 SIBP-A17获得国家药品监督管理局临床试验批准通知书。该产品拟用于在晚期恶性实体瘤患者中开展临床试验。美迪西作为上海生物制品研究所的合作伙伴,为SIBP-A17的研发提供了药代动力学和安全性评价等临床前研究服务。
2025年3月5日,山西纳安生物科技股份有限公司宣布,其自主研发的T320-ADC新药同时获得中国国家药品监督管理局(NMPA)、美国食品药品监督管理局(FDA)及澳大利亚治疗商品管理局(TGA)的临床试验批件。美迪西作为纳安的合作伙伴,为T320提供了药效、药代、安评以及生物学等临床前研究服务。
美迪西作为宜联生物的长期合作伙伴,为靶向B7H3的抗体偶联药物(ADC)YL201项目提供了高效的FTE(全时当量)服务,助力客户实现目标分子的高效研发与优化。
多禧生物的DXC014是一种创新型双抗ADC药物,靶向B7-H3和PSMA,以拓扑异构酶I抑制剂为有效载荷。该双靶点设计旨在增强对多种实体瘤(尤其是前列腺癌)的治疗效果。美迪西为DXC014提供了非临床药代动力学研究与安全性评价服务。
HX111是翰思艾泰自主研发的OX40靶向抗体偶联药物(ADC)。作为其合作伙伴,美迪西为HX111提供了临床前安全性评价服务,支持该创新ADC药物的研发。
 解决方案
解决方案 Payloads开发
Payloads开发 美迪西高活性实验室
美迪西高活性实验室 专业偶联
专业偶联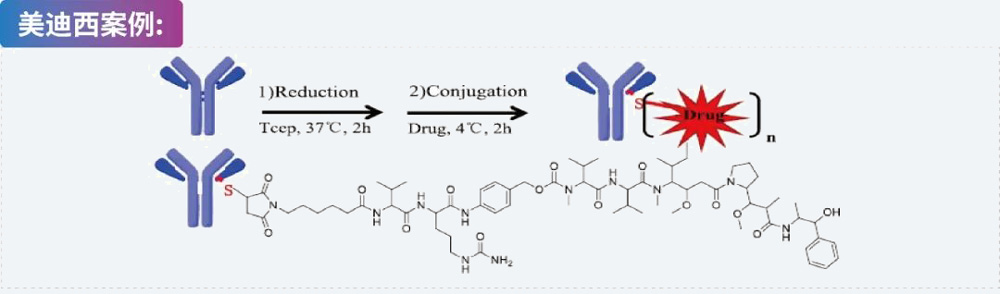 提供5 mg、50 mg、500 mg等抗体量级的偶联服务,实验周期:2-4周。QC方法包括SEC、HIC、LC-MS/MS等。DAR值≈4。提供其它偶联方法的开发服务。
提供5 mg、50 mg、500 mg等抗体量级的偶联服务,实验周期:2-4周。QC方法包括SEC、HIC、LC-MS/MS等。DAR值≈4。提供其它偶联方法的开发服务。 ADC药物体外研究
ADC药物体外研究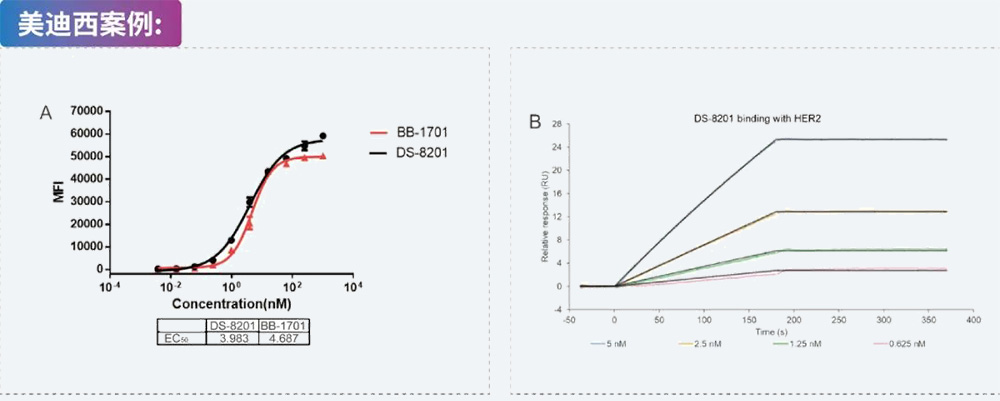 将HER2蛋白固定在M5芯片上,将DS-8201梯度稀释后注入芯片,S P R 分析(通过Biacore 8K)分析HER2和DS-8201的结合亲和力。提供ELISA, HTRF等其它方法的结合能力测试。美迪西案例:ADC内吞实验
将HER2蛋白固定在M5芯片上,将DS-8201梯度稀释后注入芯片,S P R 分析(通过Biacore 8K)分析HER2和DS-8201的结合亲和力。提供ELISA, HTRF等其它方法的结合能力测试。美迪西案例:ADC内吞实验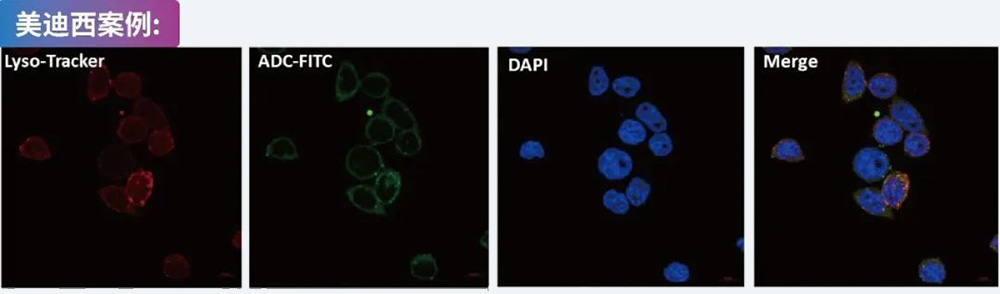 OVCAR-3 细胞与 FITC 标记的 ADC 孵育 24 小时,再与 Lyso-Tracker 和 DAPI 一起孵育,然后通过共聚焦显微镜进行分析案例分享:我们的专业能力已在多个成功项目中得到验证。精准合成与先进分析表征相结合,确保产品质量、纯度及全程可控。美迪西案例:细胞毒性测试
OVCAR-3 细胞与 FITC 标记的 ADC 孵育 24 小时,再与 Lyso-Tracker 和 DAPI 一起孵育,然后通过共聚焦显微镜进行分析案例分享:我们的专业能力已在多个成功项目中得到验证。精准合成与先进分析表征相结合,确保产品质量、纯度及全程可控。美迪西案例:细胞毒性测试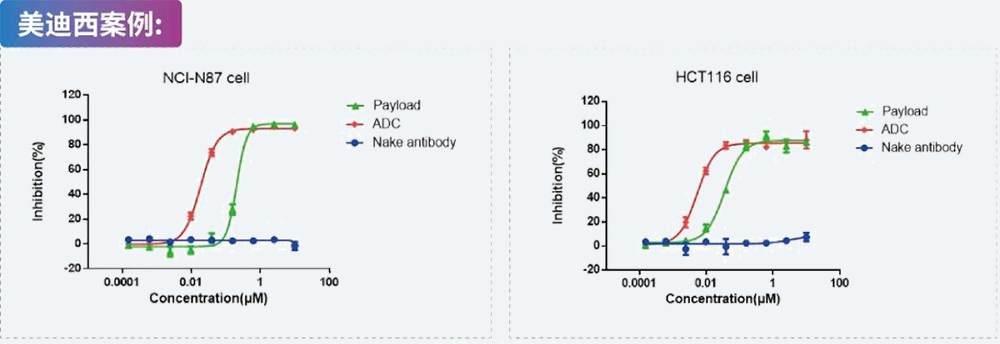 ADC、裸抗及payload与靶细胞共孵育,通过CCK-8、CTG、MTT等方法测试各个待测物对肿瘤细胞的毒性。美迪西案例:细胞周期检测
ADC、裸抗及payload与靶细胞共孵育,通过CCK-8、CTG、MTT等方法测试各个待测物对肿瘤细胞的毒性。美迪西案例:细胞周期检测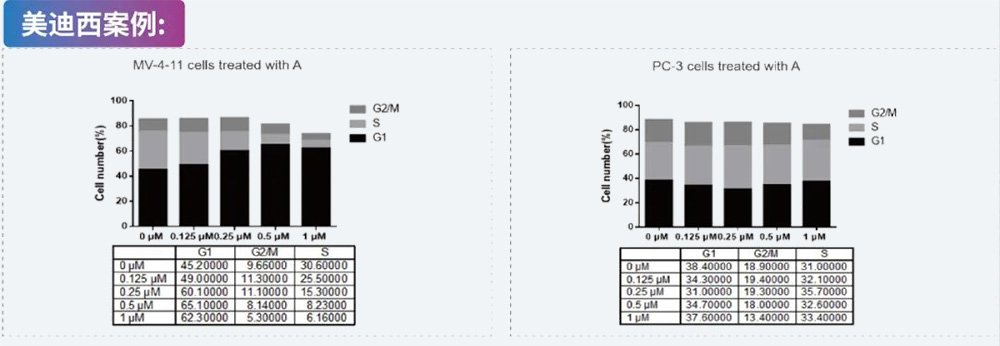 人髓性单核细胞白血病细胞MV-4-11和人前列腺癌细胞PC-3用Compound A处理并用PI染色,进行基于FACS的细胞周期分析。数据显示Compound A显著阻断MV-4-11细胞周期,对PC-3细胞没有太大影响。说明Compound A具有适应症特异性。美迪西案例: 细胞凋亡实验
人髓性单核细胞白血病细胞MV-4-11和人前列腺癌细胞PC-3用Compound A处理并用PI染色,进行基于FACS的细胞周期分析。数据显示Compound A显著阻断MV-4-11细胞周期,对PC-3细胞没有太大影响。说明Compound A具有适应症特异性。美迪西案例: 细胞凋亡实验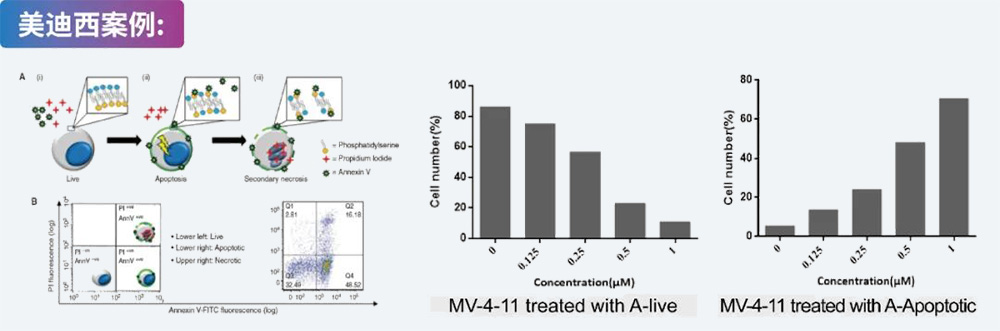 MV-4-11细胞用Compound A处理并使用 PI/Annexin V染色,然后进行 FACS 分析。 数据显示Compound A促进MV-4-11细胞凋亡。
MV-4-11细胞用Compound A处理并使用 PI/Annexin V染色,然后进行 FACS 分析。 数据显示Compound A促进MV-4-11细胞凋亡。 ADC药理药效研究
ADC药理药效研究 ADC药代动力学评价
ADC药代动力学评价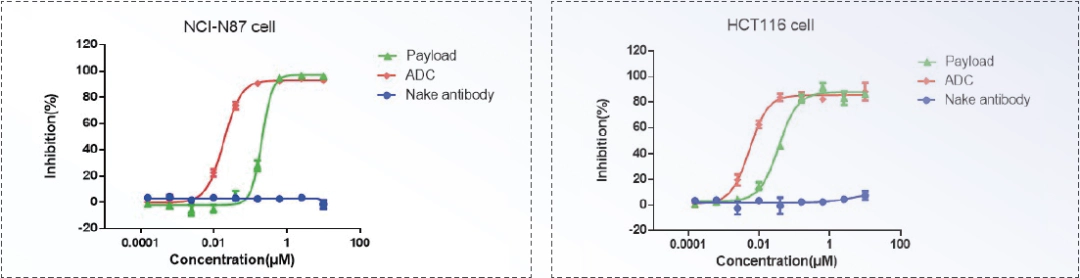 Benchmarking with global lab standard for results with high consistency. Developing stable and reliable methods for results with high correlation
Benchmarking with global lab standard for results with high consistency. Developing stable and reliable methods for results with high correlation ADC安全性评价
ADC安全性评价 美迪西部分助力ADC项目案例
美迪西部分助力ADC项目案例