 脂质体,作为一种由磷脂双分子层构成的微型泡囊,自上世纪60年代被提出以来,便因其独特的药物递送特性而备受关注。脂质体药物凭借其独特的优势,如提高药物溶解度、改善药物稳定性、增强药物靶向性等,在医药领域展现出巨大的发展潜力。
脂质体,作为一种由磷脂双分子层构成的微型泡囊,自上世纪60年代被提出以来,便因其独特的药物递送特性而备受关注。脂质体药物凭借其独特的优势,如提高药物溶解度、改善药物稳定性、增强药物靶向性等,在医药领域展现出巨大的发展潜力。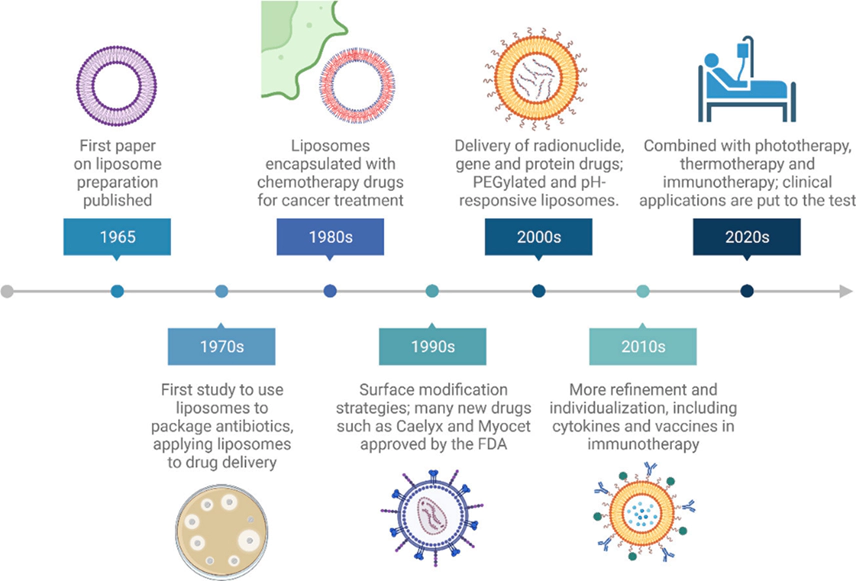 https://doi.org/10.1016/j.ejps.2023.106688
https://doi.org/10.1016/j.ejps.2023.106688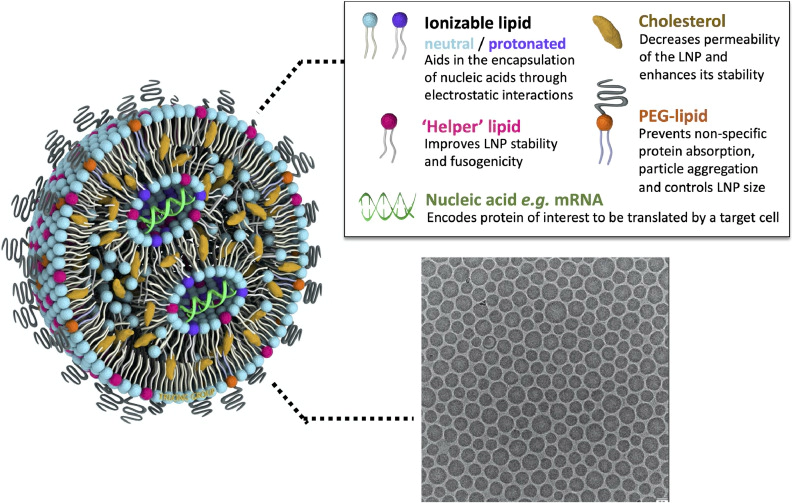 https://doi.org/10.1016/j.ejps.2023.106688
https://doi.org/10.1016/j.ejps.2023.106688
 脂质体分离制备
脂质体分离制备制备分析液相系统
配备了先进的 Thermo U3000-CAD检测系统,灵敏度高。 案例:脂质体化合物(Lipids)的制备案例脂质体化合物,无紫外,疏水性比较强,采用Waters 2545-Qda//UV/ELSD制备液相系统进行制备,结合质谱信息,使用DAD/ELSD引导收集, 分离后纯度可达98%以上。
案例:脂质体化合物(Lipids)的制备案例脂质体化合物,无紫外,疏水性比较强,采用Waters 2545-Qda//UV/ELSD制备液相系统进行制备,结合质谱信息,使用DAD/ELSD引导收集, 分离后纯度可达98%以上。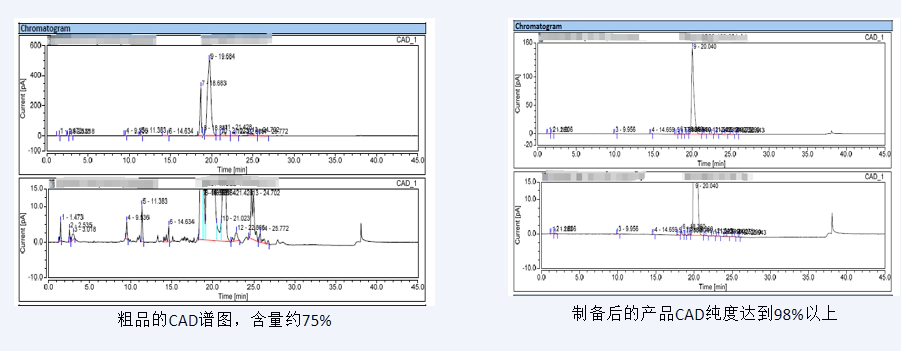
 脂质体纳米微粒制备
脂质体纳米微粒制备- 美迪西可根据以下制备方法,提供脂质体纳米微粒制备服务。
1 溶剂注入法(Solvent injection method)
溶剂注入法是一种比较简单制备脂质体的方法,将脂质成分溶解在有机溶剂中,然后将所需的药物以一定速率注射到有机相中以诱导脂质体的形成。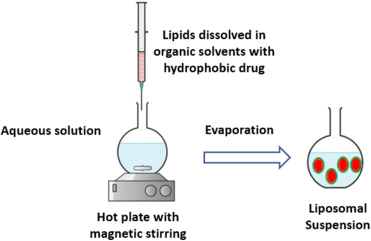 https://doi.org/10.1016/j.heliyon.2022.e09394
https://doi.org/10.1016/j.heliyon.2022.e093942 薄膜分散法(Thin-layer dispersion)
薄膜分散法简单易操作,将药物和脂质溶于有机溶剂后,置于旋转蒸发仪上减压除去溶剂,使脂质在容器壁上形成薄膜,再加入合适的水性介质,使脂质薄膜水化脱落即可制备载药脂质体。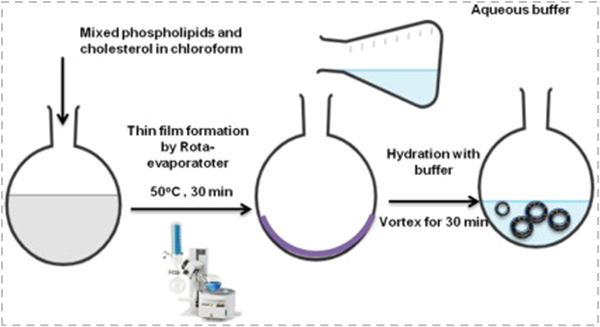 https://doi.org/10.1016/j.heliyon.2022.e09394
https://doi.org/10.1016/j.heliyon.2022.e093943 逆向蒸发法(Reverse-phase evaporation technique)
一般是将膜材的有机溶液与药物水溶液超声形成W/O型乳液,再减压蒸发,就可得到脂质体。此法适用于水溶性药物和大分子活性物质。4 挤出法(Extrusion)
挤出法即脂质体通过外力的作用,挤压通过孔径小于自身粒径的滤膜时,由于剪切力的作用导致其发生形变,从而产生破裂,随后破裂的双层立即重新结合,形成更小的脂质体。5 微流控(Microfluidic)技术
微流控制备脂质体是一种高效快速的方法,该技术通过精确控制微流体在微通道中的流动和混合,实现了脂质体的高精度、高均一性的制备。美迪西脂质体制备及分析设备
美迪西拥有的设备体系能够全面覆盖脂质体药物的研发流程,从处方筛选到制备工艺优化,再到详尽的性能分析与质量控制,尽可能满足客户需求。
 脂质体药物质量研究
脂质体药物质量研究- 美迪西可提供以下专业服务:
1 脂质体药物的结构或功能性成分的质量控制
2 脂质体药物的质量研究与控制:
(1) 鉴别、含量测定和脂质相关降解产物检查
(2) 粒径及其分布、包封率、表面电荷、体外药物释放和药物泄漏;结构和形态、脂膜的热力学性质、包封体积、包封药物的状态
(3) 其他:pH值、脂质体药物的药脂比、粘度、无菌、热原/细菌内毒素3 脂质体药物的质量标准:
(1) 性状
(2) 鉴别(API、结构或功能性成分(包括脂质和非脂质))
(3) 检查(pH、渗透压摩尔浓度、表面电荷、粒径及其分布、浊度、包封率、体外释放率、有关物质、脂质相关降解产物、装量、残留溶剂、可见异物、不溶性微粒、无菌、细菌内毒素)
(4) 含量(API、结构或功能性成分(包括脂质和非脂质))4 脂质体药物的稳定性研究:
(1) 性状
(2) 检查(pH、渗透压摩尔浓度、表面电荷、粒径及其分布、浊度、包封率、体外释放率、有关物质、脂质相关降解产物、可见异物、不溶性微粒、无菌、细菌内毒素)
含量(API、结构或功能性成分(包括脂质和非脂质))案例:脑靶向脂质体研发美迪西与美国南加州大学(University of Southern California)携手,开发一种脑靶向脂质体药物递送系统。这一合作项目将美迪西在药物制剂研发领域的深厚积累与南加州大学在神经科学方面的卓越研究能力进行结合,共同致力于解决药物递送领域的一大难题——如何有效跨越血脑屏障(Blood-Brain Barrier, BBB),以实现中枢神经系统疾病(如阿尔茨海默病、帕金森病、脑肿瘤等)的精准治疗。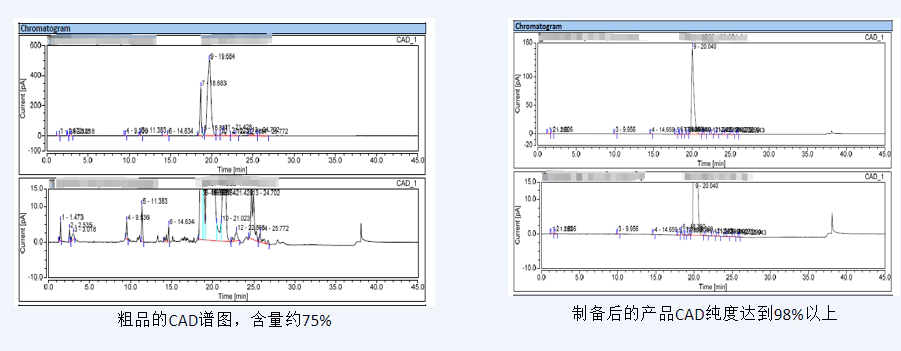
 脂质体包载药物(左)及对照(右)
脂质体包载药物(左)及对照(右)
 脂质体药物非临床安全性评价
脂质体药物非临床安全性评价- 纳米药物在体内可能通过被动靶向、主动靶向、物理靶向、化学靶向等方式高选择性地分于特定的器官、组织、细胞、细胞内结构,改变原形药物的药代动力学特征如体内组织分布,并进而影响其安全性和有效性。
1 试验系统
可先开展体外试验进行早期筛选和安全性风险预评估如细胞摄取及相互作用、补体激活情况等研究。应选择对毒性敏感的种属。2 受试物
可先开展体外试验进行早期筛选和安全性风险预评估如细胞摄取及相互作用、补体激活情况等研究。应选择对毒性敏感的种属。应提供生产过程、关键质量特征、制剂等方面的信息,如稳定性(药物和载体的化学稳定性、物理稳定性)、分散剂 /分散方法、纳米特性(粒径、粒径分布、比表面积、表面电荷、表面配体等)、表面性质(包衣及厚度、配体及密度等)、载药量、浓度、溶解性、药物从载体的释放、纳米药物的聚集状态及变化过程、表征的方法和检测标准等。若纳米药物需稀释和/或配制后给药,应关注纳米药物配制后在不同浓度、溶媒、体外细胞培养液或者其它体外试验体系下的稳定性、均一性和药物释放率等特征是否发生改变。3 试验设计
给药剂量:除采用传统的质量浓度外可考虑同时提供质量浓度和纳米颗粒数目/比表面积的剂量单位信息。
对照组:包含新药物活性成分的,设单独的药物活性成分组;包含新纳米载体的,设无药纳米载体组。
检测时间和频率:可能在组织中清除慢,根据蓄积情况设置检测时间点和检测频率,必要时延长恢复期。4 毒性关注点
免疫原性和免疫毒性:纳米药物主要经单核吞细胞系统的吞细胞洁除,聚集到肝脏、脾脏和淋巴组织等器官组织 。可能吸附不同生物分子(以蛋白质分子为主)形成生物分子层(如蛋白冠),进而被免疫细胞表面受体识别,产生免疫原性和免疫毒性,还可导致类过敏反应。可能存在免疫增强、免疫抑制、补体活化、炎反应、过敏反应、细胞因子释放等风险。参考ICH S8。
神经系统毒性:纳米药物与普通药物相比更容易透过血脑屏障,有神经毒性风险的药物应进行安全药理试验评估对神经系统的影响。
遗传毒性:新药物活性成分的纳米药物和新纳米载体/辅料需要开展遗传毒性评价。
生殖毒性:纳米药物可能容易通过胎盘屏障、血睾屏障、血乳屏障等生物屏障,因此应关注生殖毒性风险,参考ICH S5。
致癌性:参考ICH S1(长期使用的需进行)。
制剂安全性:同注射剂要求,体外溶血试验应注意,若纳米药物在溶液中会发生团聚,建议进行体内溶血试验。
毒代动力学:部分纳米药物可能在组织中存留的时间较长,组织暴露量高于系统暴露量,在体内某些组织器官发生蓄积,重复给药后可能产生明显的毒性反应。5 不同给药途径的特殊关注点
经皮给药:纳米药物可能具有较高的毛囊渗透性或分布至局部淋巴结。毒性试验中应注意考察不同皮肤状态(完整、破损、患病)、不同影响因素下(如光照)纳米药物在给药局部和全身的暴露量差异以及相应的毒性风险。
皮下给药:具有更高致敏潜力。需关注不溶性纳米药物在皮下的蓄积和转移以及相应的毒性风险。
鼻腔给药:相比胃粘膜更有利于药物吸收,可能通过嗅神经通路透过血脑屏障。
吸入给药:纳米药物可广泛分布于肺泡表面,应关注局部/呼吸毒性。应关注不溶性载体类纳米药物在肺部的蓄积和转移。
静脉给药:与普通药物不同的组织分布与半衰期。
口服给药:不溶性纳米成分可能蓄积在某些组织。美迪西可提供以上多种给药方式的纳米药物的非临床安全性评价,包括符合NMPA、FDA法规申报要求的一般毒性研究、药代/毒代动力学研究,免疫原性/免疫毒性评估、制剂安全性研究、遗传/生殖毒性研究、致癌性研究等。
 脂质体药物药代动力学研究
脂质体药物药代动力学研究- 通过药代动力学研究,美迪西能够准确评估脂质体药物在体内的吸收、分布、代谢和排泄过程,为药物的优化提供科学依据。载体类纳米药物需要分别测定血液中游离药物和负载型药物(总药物)的浓度。某些载体类纳米药物(如PEG化的)静脉注射后可诱导免疫反应,重复给药后会加速清除,并在肝脾等组织聚集量增加。即加速血液清除(Accelerated Blood Clearance,ABC)现象。此类载体类纳米药物在多次给药试验时,建议考察是否存在ABC现象(如抗PEG抗体)。
1 分布:
纳米药物在组织器官中的分布取决于载药粒子自身的物理化学性质及其表面特性;同时,还受到血中蛋白结合。组织器官血液动力学、血管组织形态(如问隙大小)等多种因素的影响。其中载药粒子是药物的运输工具和储库,靶部位/靶点(如肿瘤组织)中的游离药物是发挥药效的物质基础,而其他组织中的游离药物、我药粒子、载体材料等则可能是导致毒性/不良反应的物质基础。因此,应进行不同组织中总药物分布研究,如可行,建议对靶器官和潜在毒性器官中的游离型药物和负载型药物分别进行测定。对于缓慢生物降解或具有明显穿透生理屏障性质的高分子载体材料,建议进行不同组织中总载体材料的分布研究。同时,鼓励在不同组织中进行总粒子分布动力学和释药动力学研究。2 代谢:
载体类纳米药物中的活性药物及其解聚的载体材料在体内主要经肝脏和其它组织中的代谢酶代谢。此外载药粒子易被MPS吞噬,进而被溶酶体降解或代谢,可能对药物和载体材料代谢/降解产物的种类和数量产生影响。因此,应确定活性药物和载体材料的主要代谢/降解途径,并对其代谢/降解产物进行分析。3 排泄:
载体类纳米药物中的活性药物和载体材料可能通过肾小球滤过和肾小管分泌进入尿液而排泄,或通过肝脏以胆汁分泌形式随粪便排泄。载药粒子自身一般不易经过上述途径直接排泄,需解聚成载体材料或载体材料降解后主要经肾脏排泄。因此,应确定给药后活性药物的排泄途径、排泄速率及物质平衡。同时鉴于载体材料的特殊性,建议根据载体材料的具体情况对其开展排泄研究。案例 脂质体化合物(Lipids)的制备案例适应症 肿瘤 给药途径 静脉注射 研发目的 1.增强药效,降低剂量。2.降低毒性反应。 对照组 溶媒对照、空白脂质体对照、普通注射液(非脂质体)对照解放热量很大,潜在爆炸危险性很高。 剂量 参考普通注射液毒性及预实验设计,脂质体高剂量与普通注射液剂量相同 大鼠TK:同剂量下,脂质体组游离药物与普通注射液血浆暴露量对比,Cmax降低,但AUC(0-144h)更高,脂质体包裹的药物具有一定缓释作用。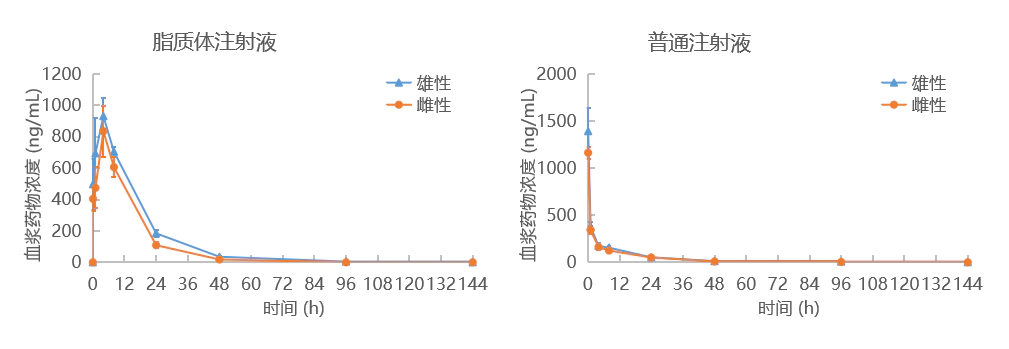 荷瘤小鼠组织分布:同剂量下,脂质体与普通注射液相比,药物在肿瘤组织中的蓄积量更高,可以更好地发挥药效。
荷瘤小鼠组织分布:同剂量下,脂质体与普通注射液相比,药物在肿瘤组织中的蓄积量更高,可以更好地发挥药效。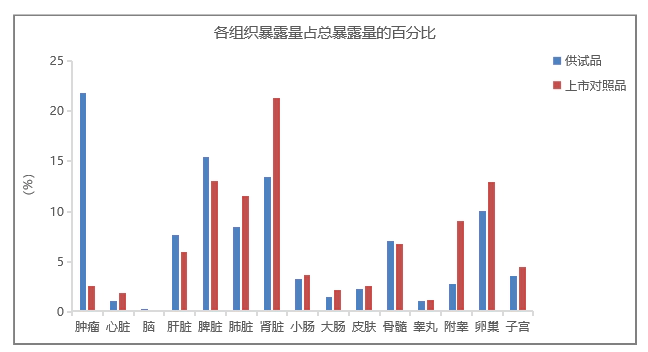
 脂质体药物生物分析
脂质体药物生物分析- 平台采用先进的生物分析技术,对脂质体药物进行精确的定量分析,为药物研发提供有力支持。服务内容:开展药代动力学(PK)和毒代动力学(TK)样本生物分析工作;全方位支持从早期筛选到临床前以及临床各阶段的生物分析。
1 生物分析方法开发和验证
(1) 脂质体目标分析物
指导原则指出进行药代动力学研究时需测定生物样本中负载型(或总药物)和游离型(完全游离+蛋白结合)药物浓度(2) 前处理技术
蛋白沉淀(PPT):破坏蛋白质分子的水化作用或者减弱分子间同性相斥作用的因子,使蛋白质在水中的溶解度降低而沉降下来转化为固体的分离方法。常用有机试剂沉淀、等电点沉淀、盐析等。
液液萃取(LLE):根据化合物极性不同,采用相似相容原理,将分析物或不需要的干扰成分从一个液相(如生物样品)提取到另一个不混溶液相(如有机溶剂),从而进行样品清理。常用溶剂有正己烷、甲基叔丁基醚、正丁醇和乙酸乙酯等。
固相萃取(SPE):机理类似于液相色谱,通过溶解在液体中的溶质(分析物)与吸附剂材料(固定相)之间的亲和力或相互作用实现。常用有反向SPE、离子交换SPE。
超滤:超滤是一种加压膜分离技术,即在一定的压力下,使小分子溶质和溶剂穿过一定孔径的特制的薄膜,而使大分子溶质不能透过,留在膜的一边,从而使大分子物质得到了部分的纯化。常用为超滤管。
此外还有平衡透析、超速离心、排阻色谱、柱切换色谱等分离方法。固相萃取(SPE)
SPE 的大致流程:样品准备→活化→平衡→上样→淋洗→洗脱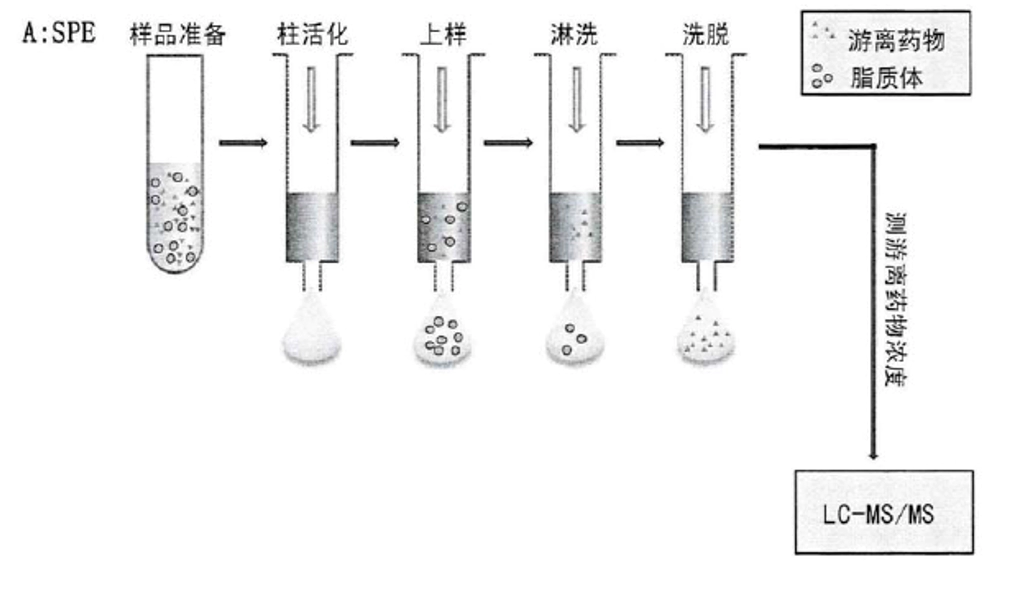
2 生物基质样本分析
不同生物基质测定
指导原则中建议对血浆和组织样品中总药物和游离药物浓度进行测定。但是目前组织还是采用物理匀浆处理的方式对样品进行处理,这势必会造成脂质体的破碎,所以,现阶段技术手段还做不到组织中游离药物浓度的检测。基质 总药物 游离药物 大鼠血浆 需要 需要 犬血浆 需要 需要 猴血浆 需要 需要 小鼠血浆 需要 需要 大鼠组织 需要 小鼠组织 需要 大鼠排泄 需要
 更多“脂质体药物研发”相关内容推荐
更多“脂质体药物研发”相关内容推荐- 推荐阅读:(1) 美迪西核酸药物研发服务平台(4) 美迪西抗体药物研发服务平台












 查看更多服务案例
查看更多服务案例






