




2023年11月28日,FDA宣布调查靶向BCMA或CD19的自体CAR-T细胞免疫治疗后患者出现T细胞恶性肿瘤的严重风险。这条“风险提示”适用于所有目前已获FDA批准的靶向BCMA或CD19的自体CAR-T细胞免疫疗法。
CAR-T在血液肿瘤领域展示了非常强大的疗效和很好的获益风险比,前景有目共睹,但持续关注其潜在风险的举措是必须的。
目前,FDA正在调查上报的T细胞恶性肿瘤严重不良反应事件,并评估下一步监管行动的必要性。

CD19在正常和肿瘤B细胞以及滤泡树突状细胞中特异性表达,而在造血干细胞、浆细胞、T细胞及其他组织中则没有表达。
聚焦自身免疫性疾病和癌症治疗领域
❖ Kymriah(tisagenlecleucel),诺华:全球首个上市,三个适应证均已获FDA批准,并且是目前唯一一个同时覆盖成人和儿科人群的CAR-T细胞疗法。
获批适应症:①先前接受过二线或以上系统治疗的复发/难治性滤泡性淋巴瘤(r/r FL)成人患者;②复发/难治性急性淋巴细胞白血病(r/ALL)儿童和年轻成人患者(年龄至25岁);③复发/难治性弥漫性大B细胞淋巴瘤(r/r DLBCL)成人患者。
❖ Yescarta(axicabtagene ciloleucel),Kite Pharma(吉利德科学旗下):于2017年10月FDA批准上市,全球首个针对既往接受过二线或以上系统性治疗后复发/难治性的大B细胞淋巴瘤成人患者的CAR-T疗法产品。
❖ Tecartus(brexucabtagene autoleucel),同样来自Kite Pharma:2020年7月获FDA批准,全球首款应用于治疗复发/难治性套细胞淋巴瘤成人患者,并在次年获批治疗复发/难治性B细胞急性淋巴细胞白血病成人患者。
❖ Breyanzi(lisocabtagene maraleucel),百时美施贵宝,2021年2月获FDA批准,用于治疗接受过两种或以上系统治疗的复发/难治性大B细胞淋巴瘤成人患者。今年6月,公布治疗复发/难治性滤泡性淋巴瘤患者的全球多中心II期试验(NCT04245839)研究数据,完全缓解率CR达94%。
B细胞成熟抗原 (BCMA, B cell maturation antigen) 是肿瘤坏死因子受体(TNFR)超家族的成员,几乎只在浆母细胞和浆细胞上表达。
治疗骨髓瘤的明星靶点
❖ Abecma(idecabtagene vicleucel),百时美施贵宝:FIC、BCMA导向、个体化免疫细胞疗法,2021年获FDA批准, 用于治疗既往至少接受过4线治疗无效或复发的多发性骨髓瘤成人患者,既往治疗需包括:免疫调节剂、蛋白酶抑制剂和抗CD38单克隆抗体药物的治疗。目前,用于三线治疗复发/难治性多发性骨髓瘤的申请正在审批中。
❖ Carvykti(ciltacabtagene autoleucel),传奇生物和强生:首个国内自主研发,且在海外获批上市的细胞疗法。于2022年获FDA批准,因疗效的优异表现,已被行业冠以BIC之名。
FDA在此次发文中特别强调,CAR-T疗法总体的益处远大于风险,所以撤回已获批产品的可能性极小。第一代CAR-T诞生至今仅30余年,我们可以将本次“考验”看作“螺旋式上升”发展过程中的一道弯,并重点关注热度过后平衡风险的策略。
FDA在公告中指出,逆转录病毒载体的使用可能会增加继发性癌症的风险。这些是经过修饰的病毒,携带遗传负荷(此次事件里为CAR基因),并将其整合到T细胞的基因组中。纪念斯隆·凯特琳癌症中心的计算免疫学家Caleb Lareau则表示,问题可能在于科学家无法精确控制逆转录病毒在基因组中的位置。
CAR-T细胞疗法为血液系统恶性肿瘤带来治愈可能性的同时,上百亿T细胞短时间输注到患者体内,有一定几率带来潜在毒性风险。
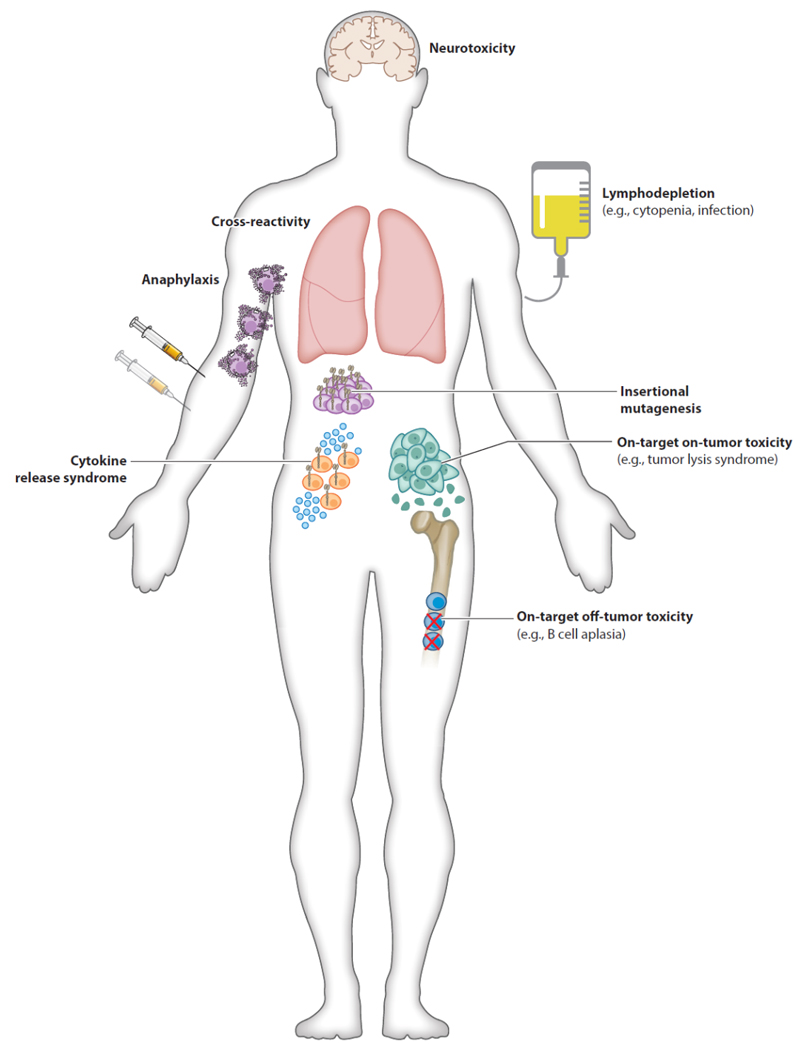
与CAR-T细胞疗法相关的潜在毒性
❖ CRS 细胞因子释放综合征:与CAR-T细胞治疗相关的主要毒副作用之一。大量免疫细胞的快速激活,导致高水平的全身炎症细胞因子,进而引起机体损伤。
❖ Neurotoxicity 神经毒性:继CRS之后,神经毒性是与CAR-T细胞治疗相关的第二常见不良事件。由于与CRS相比,ICANS(免疫效应细胞相关神经毒性综合征)对干预的时间和反应不同。
❖ 淋巴清除引起的相关毒性:CAR-T治疗前会进行淋巴细胞清除,减少调节性T细胞数量,增加细胞因子(尤其是IL-2)可用性,降低免疫排斥反应。相关毒性反应包括:中性粒细胞减少、白细胞减少、贫血和血小板减少的血液毒性,也会增加感染的机率。
❖ On-Target Off-Tumor:这是在CAR-T治疗中较为常见的毒性反应,通常由于靶点在正常组织内同样表达,会被CAR-T识别并攻击而引起。
❖ On-Target On-Tumor:CAR-T识别肿瘤细胞靶分子后并迅速破坏,随着内容物在血液中突然释放,会导致代谢紊乱并影响器官功能,这种现象被称为肿瘤溶解综合征。虽然不常见,但在慢性淋巴细胞白血病和B-ALL患者中都有相关案件报道。
❖ Anaphylaxis 过敏反应:随着越来越多全人源scFv的使用,这类识别外来成分(小鼠衍生的scFv序列)反应的风险会降低。
❖ Insertional Mutagenesisi 插入突变:CAR是基因修饰产品,存在插入突变的可能性。但就当前情况,该副作用基本没有发生,并陆续出现转座子等更安全的方式,开展基因转导相关的临床试验。
CAR-T疗法正持续拓展实体瘤、自身免疫疾病、HIV感染等适应症的应用空间。除了探索更合适的递送载体,尽量避免使用整合型的载体,还需要更加关注此类创新药物的安全性评价工作,特别是在非临床阶段,重视潜在脱靶毒性和插入突变等评估。
细胞治疗药物的非临床安全性研究主要针对药物潜在的安全性风险而设计展开。以Kymriah免疫原性检测方法为例,由于Kymriah细胞疗法中患者来源的CAR-T细胞数量非常有限,无法建立患者特异性免疫原性测定方法,考虑给药类似的接近理想体系的目的,建立了一个颇为复杂、也是第一种基于细胞的体液免疫原性试验方法。

CAR特异性ADA信号等于CAR19细胞检出的信号与WT细胞的非特异性信号之间的差值
在原文末作者也提到,应该考虑使用比较简单的方法来检测CAR-T疗法的免疫原性。后续几款抗CD19 CAR-T产品的上市,也证明了无论是采取基于细胞的方法,还是采取配体结合试验(如使用ELISA平台),只要能够说明患者体内的免疫原性对CAR-T细胞的初始扩增和持续存在的动力学、药物的安全性和有效性、和重复给药等治疗过程未造成影响,这样的免疫原性的分析方法和分析结果也是可以得到审核机构认可和接受的。
2023年2月,英百瑞的IBR854细胞注射液获得国家药监局临床试验默示许可。IBR854注射液是同源异体外周血来源的通用现货型CAR-raNK细胞产品,适应症为不可切除的局部晚期或转移性且目前无或不耐受标准治疗的实体肿瘤患者的治疗,是针对实体肿瘤的非基因修饰方法的CAR-raNK细胞疗法。
美迪西作为英百瑞的合作伙伴,为IBR854细胞注射液提供了符合GLP规范的(包括药物动力学研究和安全性评价)综合性临床前研究服务,以合规、高效、高质的服务助力其顺利获批。
体外生物学活性检测作为生物制品临床申报的必检项,在方法开发、人员操作稳定性以及实验室合规管理等方面都有极高的要求。
美迪西的细胞活性检测平台可提供符合申报要求的合规性体外细胞活性检测服务,高水平的科研团队可协助客户参与新药研发与药物作用机制探索,高通量的筛选平台可帮助客户进行高效的药物筛选。
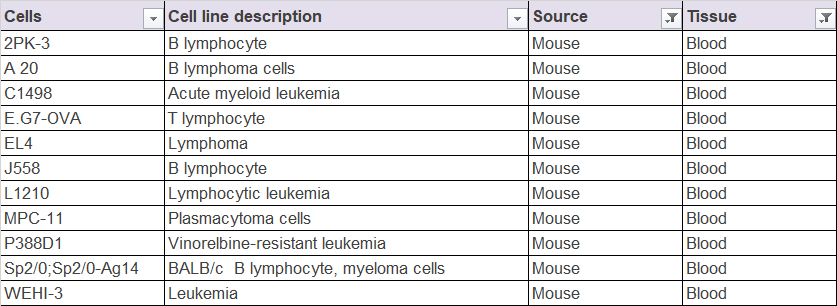
图源:美迪西官网公开资料
如您对本期话题有进一步想要了解的内容,或您希望美迪西Marketing讨论更多行业资讯,欢迎点击:文章最下方「发消息」给我们留言互动。期待您的"美"思妙想~
1. https://www.fda.gov/vaccines-blood-biologics/safety-availability-biologics/fda-investigating-serious-risk-t-cell-malignancy-following-bcma-directed-or-cd19-directed-autologous
2. Andrea Schmidts et al,Toward Better Understanding and Management of CAR-T Cell–Associated Toxicity,Annu. Rev. Med. 2021. 72:7.1–7.18
3. https://mp.weixin.qq.com/s/3j77bLcx88nwSB853G2Izg,诺华Kymriah®疗法免疫原性分析方法简介
 相关新闻
相关新闻