



最近,【自然癌症进展】上发表评论文章,称巨噬细胞“窃用”了免疫疗法的大秀台 [1]。这个说法主要是基于最近的两篇报道发现巨噬细胞跟PD-1的联系比我们以前以为的要更加密切。首先是Pittet等人报道巨噬细胞会识别并“扣留“、吞噬作为治疗用的PD-1抗体,从而降低其疗效[2]。而Weissman等人则报道从肠癌等样品中分离的巨噬细胞,其中很大的部分表面含有PD-1抗原,这些被肿瘤“驯服”的M2类型的巨噬细胞吞噬肿瘤细胞的能力由此大大降低[3]。
与“专业选手”T细胞相比,巨噬细胞这个“业余选手”也能搭建自己的抗肿瘤舞台吗?
早在1970年代,就有报道提到细胞或细胞因子激活的巨噬细胞具有抗肿瘤活性[4]。但在同时,却也有报道发现肿瘤相关的巨噬细胞(TAM)能够促进癌细胞的生长和转移[5]。这与巨噬细胞本身的正常生理功能其实是吻合的。巨噬细胞根据功能和极性分类,可笼统分为M1和M2两大类型(最新报道,细分起来,有超过20几类还多)。M1主要参与炎症反应,识别、吞噬外来入侵物(包括变异肿瘤细胞)及清除体内细胞碎片。M2主要参与免疫抑制及愈伤组织修复 [6]。
体现在对肿瘤关系上,巨噬细胞就是有时杀伤肿瘤,经常辅助肿瘤生长转移,总是骑墙派。
或者说巨噬细胞“匪性”很强,农忙时回家种地促生产,农闲时打家劫舍搞破坏,具有阴阳双性。
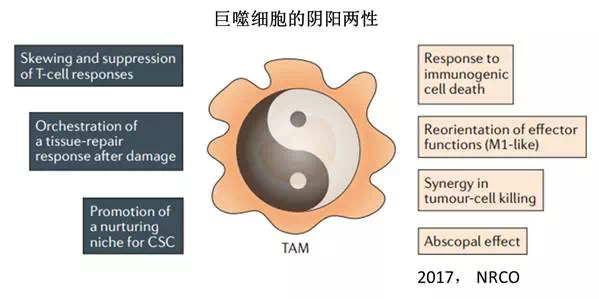
巨噬细胞的极性取决于疾病发生的阶段,所涉及的组织,甚至宿主微生物的状态。个人感觉,早期的肿瘤微环境,至少部分巨噬细胞可能更倾向于积极的抗肿瘤免疫反应,晚期的肿瘤,巨噬细胞被多被肿瘤细胞欺骗,诱惑,收编,更多的倾向于支持肿瘤细胞生长,转移,并抑制积极的免疫反应。
绝大多数情况下,肿瘤相关巨噬细胞都是“从犯”,“协犯”,不是主要致癌因素,所以更多时候靶向TAM是帮助、教育它转性,从M2类型转化成M1类型,让巨噬细胞从助癌变成抑癌,而不是杀死巨噬细胞。当然,个例也是存在的,下面会有讨论。
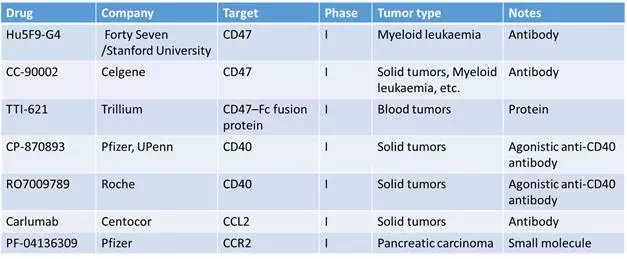
靶向巨噬细胞的潜在靶点较多,临床上进展较快的主要靶点有:CSF-1R、CD47、CD40、巨噬细胞微环境趋化因子等。
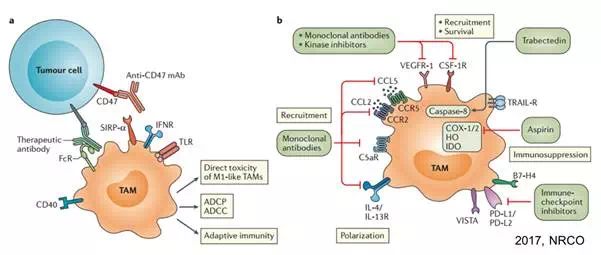
迄今为止,还没有直接靶向巨噬细胞的药物获得FDA批准。
CSF-1R是迄今靶向巨噬细胞研究最成熟的靶点之一。CSF-1R属于络氨酸受体激酶,仅在单核细胞系,如巨噬细胞表面表达,其主要配体之一CSF-1与之结合后可以促进巨噬细胞的生长、分化。在多种肿瘤,如乳腺癌、肝细胞癌等中发现,高CSF-1或CSF-1R表达水平与不良生存预后呈正相关。
靶向CSF-1R的策略既可以用大分子抗体靶向其CSF-1配体,或CSF-1R受体,也可以设计小分子靶向激酶活性区域。
目前临床上活跃的药物包括5个抗体、4个小分子。较为领先的抗体是Roche的Emactuzumab(RG7155),小分子是Plexxikon 的PLX-3397 [7]。
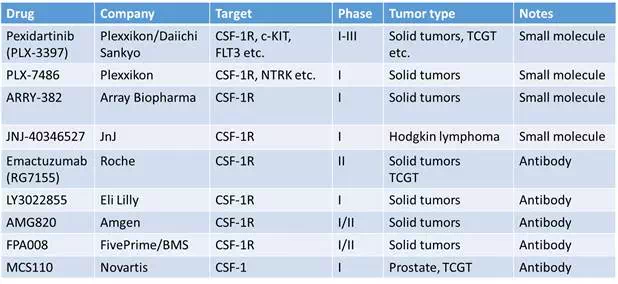
CSF-1/CSF-1R信号通路大部分情况下不是致癌驱动因素。但在一类罕见的腱鞘巨细胞瘤(TCGT,tenosynovialgiant-celltumor),CSF-1却是元凶。这类细胞瘤主要发生在关节部位,特别是膝关节。发病人群较为年轻,平均年龄为35岁左右。目前主要治疗手段是手术,但复发率比较高,患者急需新的疗法。TCGT致病机理主要是少量位于滑膜衬里的细胞由于CSF-1的染色体移位,造成其持续过量表达,从而吸引、招募过多的巨噬细胞造成的组织增生。早前,这类疾病还划归于自身免疫疾病,叫色素沉着绒毛结节性滑膜炎(PVNS,pigmentedvillonodularsynovitis),也是有道理的。临床上,这类细胞瘤是验证CSF-1/CSF-1R靶向药物有效性的理想对象[7]。
最早Imatinib就对这个疾病进行了尝试。但由于imatinib的CSF-1R的活性较弱,总体应答率较低,只有19%。
Roche的CSF-1R的抗体emactuzumab具有极高的活性。临床前的试验表明其能够有效地抑制M2类型的巨噬细胞,促进T细胞活性的增加[8]。在TCGT的临床试验中也表现出积极的应答率86%(24/28)。其中两例患者达到完全缓解[9]。进一步证明了CSF-1/CSF-1R信号通路的可靶向性。Emactuzumab的副作用主要包括面部水肿(眶周水肿)、乏力和瘙痒等。
小分子CSF-1R的激酶抑制剂在TCGT患者人群同样表现出优异的临床数据,PLX-3397的ORR达到52%(12/23)[10]。与PLX-3397相关的毒性主要包括:疲劳、头发颜色变化(74%)、恶心、味觉障碍、眶周水肿等。还不是非常确定哪些毒性是与靶向CSF-1R直接相关的。
尽管PLX-3397的选择性不错,报道的活性很高,它的PK也相当好,但它的临床试验使用剂量达到1000mg/每天。有些怀疑它的活性可能没有其报道的高。与CSF-1R抗体的更高应答率、更小毒性相比,PLX-3397 的临床患者有61%还需要通过减少剂量来降低毒性。
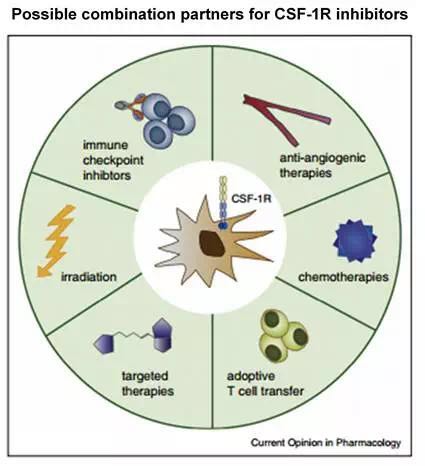
除了上面提到的TCGT,CSF-1R单用在其它诸多实体瘤的临床试验也在开展。目前得到的初步数据不是很积极,单用效果有限。CSF-1R的靶向潜力更多的应该是联合用药,与IDO抑制剂的情况类似,能不能达到IDO的联用效果还有待观察。
CD47–SIRPα信号通路在调控巨噬细胞的吞噬过程中起重要作用。SIRPα和CD47均属于免疫球蛋白超家族的成员,分别在巨噬细胞和候选目标细胞中表达。在结合CD47后,SIRPα作为对接蛋白,结合SHP1和SHP2磷酸酶,从而抑制细胞内信号,并由此负调控吞噬作用。因此,CD47的生理作用表现为发布“不要吃我”(Don’t eat me)的信号[11]。
在正常生理情况下,CD47蛋白存在于很多健康细胞的表面,通过和巨噬细胞表面的SIRPα(Signalregulatoryprotein-α)结合来告诉巨噬细胞不要去“吞吃”它们,从而保护健康细胞不被清除。当细胞老化或病变时,细胞表面就会逐渐丧失CD47,巨噬细胞从而能够识别并处理掉衰老或病变细胞[12]。
而很多肿瘤细胞学会了这个机制,经常过量表达CD47,直接导致TAM不但同肿瘤细胞能够和平共存,而且TAM还会通过促进肿瘤内血管增殖,抑制效应T细胞发挥作用,促进肿瘤细胞扩增和生长,完全把肿瘤细胞当成自身的愈伤组织来养。
靶向CD47–SIRPα通路的策略主要有两种,CD47的抗体或SIRPα–Fc重组蛋白。两种方法均得到临床前的疗效验证。目前多于4家公司正在开展临床试验。初步临床结果好像也不支持靶向CD47的单用疗效[6]。当然,靶向CD47 的潜力是要与免疫疗法如PD-1抗体合用,才能充分发挥威力,同样,道理与IDO的组合疗法类似。
同时,CD47靶向药物在临床前使用中已被证明与其它不同的抗肿瘤单克隆抗体也有协同作用,包括抗CD20和抗HER2抗体[6]。期待将来的临床组合疗法试验结果。
与靶向CSF-1R相比,靶向CD47可能会产生更多的靶向相关毒副作用。比如红细胞上有CD47高表达,打破红细胞表面的保护信号,导致巨噬细胞错误地清除健康的红细胞,从而诱发贫血症。其它细胞也有较多的CD47表达,如淋巴细胞、血小板、胎盘、肝和脑细胞等。靶向CD47 的临床试验需要密切监视对这些健康细胞,组织可能的毒性损伤。
巨噬细胞的其它靶点
肿瘤细胞可以通过表达趋化因子CCL2、CCL5、CXCL12等促进MDSC和巨噬细胞向肿瘤区域迁移,通过阻断这些招募通路,可以减少肿瘤浸润区域中的MDSC和促肿瘤特性的巨噬细胞数量[6,13]。早期临床试验表明,CCL2抗体Carlumab,在乳腺癌、肺癌等实体瘤患者中虽然可以良好耐受,单用却没有获得有效缓解。进一步表明,组合疗法才能更好的发挥靶向巨噬细胞的威力。
激动剂型的CD40抗体能够有效的转化M2巨噬细胞成为M1类型的巨噬细胞,从而起到抑制肿瘤生长、转移的作用。CP-870893与化疗药物联用,在胰腺癌临床试验中表现出不错的活性 [14]。
巨噬细胞是肿瘤先天性免疫生态的主要成分之一,在肿瘤的发生、发展和转移过程中起着关键作用。
从初步的肿瘤临床试验结果来看,巨噬细胞自搭舞台的表演机会不是很多。组合疗法,共享舞台才是巨噬细胞靶向药物的未来。好在,诸多的临床前试验表明,靶向巨噬细胞能够与各种疗法进行组合,包括化疗、放疗、免疫疗法、靶向疗法等等,是个不错的百搭靶点。其组合潜力还需要进一步临床试验来验证。
同时,肿瘤或血液中CSF-1、CSF-1R、CD47的表达量也许是不错的预测标记物,用来指导组合疗法患者的选择。在个体化治疗日益盛行的今天,有选择性的组合疗法代表着未来。
参考文献:
Immunotherapy: Macrophages steal the show. Villanueva MT. Nat Rev Cancer. 2017, June 23; 17(7):396-397.PD-1 expression by tumour associated macrophages inhibits phagocytosis and tumour immunity. Gordon, S. R. et al. 2017, Nature. 545, 495–499.
In vivo imaging reveals a tumor-associated macrophage mediated resistance pathway in anti-PD-1 therapy. Arlauckas, S. P.et al. Sci. Transl Med. 2017, 9, eaal3604.
Cooperation of immune lymphoid cells with macrophages in tumour immunity. Evans, R. & Alexander, P. Nature. 1970, 228,620–622.
Effects on in vitro tumor growth of murine macrophages isolated from sarcoma lines differing in immunogenicity and metastasizing capacity. Mantovani, A. 1978, Int. J. Cancer 22, 741–746.
Tumour-associated macrophages as treatment targets in oncology. Mantovani A, Marchesi F, Malesci A, Laghi L, Allavena P. Nat Rev Clin Oncol. 2017, Jul;14(7):399-416.
CSF-1/CSF-1R targeting agents in clinical development for cancer therapy. Ries CH, et. al. Curr Opin Pharmacol. 2015, 23:45-51.
Targeting tumor-associated macrophages with anti-CSF-1R antibody reveals a strategy for cancer therapy. Ries CH, et. al. Cancer Cell. 2014, 25(6):846-859.
CSF1R inhibition with emactuzumab in locally advanced diffuse-type tenosynovial giant cell tumours of the soft tissue: a dose-escalation and dose-expansion phase 1 study. Cassier PA et al. Lancet Oncol. 2015, 16(8):949-956.
Structure-Guided Blockade of CSF1R Kinase in Tenosynovial Giant-Cell Tumor. William D. Tap, M.D., Zev A. Wainberg, et. al. N Engl J Med. 2015, 373:428-437.
CD47-blocking antibodies restore phagocytosis and prevent atherosclerosis. Kojima Y, et al.2016, Nature 536:86-90.
CD47 blockade as another immune checkpoint therapy for cancer. Vonderheide RH. Nat Med 2015, 21:1122-1123.
Targeting tumour-associated macrophages with CCR2 inhibition in combination with FOLFIRINOX in patients with borderline resectable and locally advanced pancreatic cancer: a single-centre, open-label, dose-finding, nonrandomised, phase 1b trial. Nywening, T. M. et al. Lancet Oncol. 2016,17:651–662.
A phase I study of an agonist CD40 monoclonal antibody (CP-870,893) in combination with gemcitabine in patients with advanced pancreatic ductal adenocarcinoma. Beatty, G. L. et al. Clin. Cancer Res. 2013, 19:6286–6295.
 相关新闻
相关新闻