



2024年5月17日-19日,中国药学会核酸药物专业委员会成立大会暨核酸药物创新研究研讨会在广东省中山市隆重召开。此次盛会汇聚了国内外优秀的专家学者和企业家,共同探讨核酸药物领域的最新研究成果与发展趋势,为推动核酸药物领域的发展注入了新的活力。
作为新成立的中国药学会核酸药物专业委员会第一届委员会委员,美迪西创始人&CEO陈春麟博士受邀出席此次大会,并发表了重要演讲。

陈博士详细介绍了美迪西在核酸药物评价平台及合作模式方面的独特优势,向与会嘉宾展示了美迪西在核酸药物研发领域的深厚实力与前瞻视野。
美迪西在核酸药物研发领域积累深厚,拥有全面的临床前研究能力:强大的药物合成、修饰及递送系统研究实力,确保药物稳定性与活性;完善的生物学分析与筛选技术,迅速筛选潜力药物;专业的生物样品分析采集能力,确保数据真实可靠;丰富的非临床安全性研究经验,为药物研发提供坚实保障。
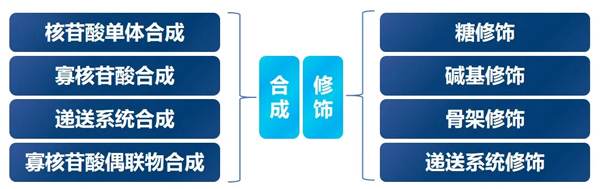
美迪西核酸药物合成服务涵盖了核苷酸单体合成/寡核苷酸合成/递送系统合成以及寡核苷酸偶联物合成等。
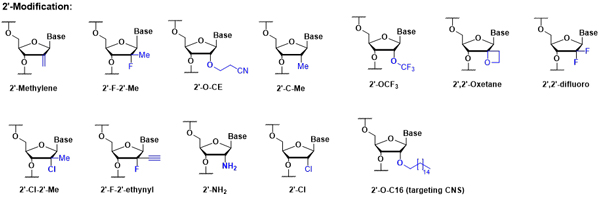
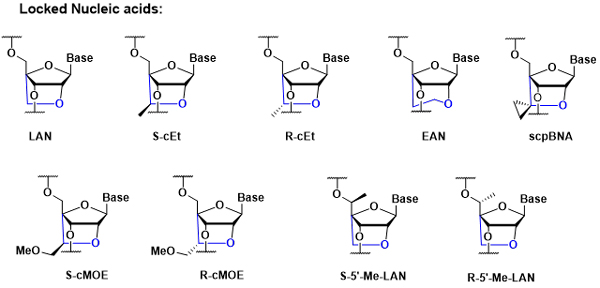
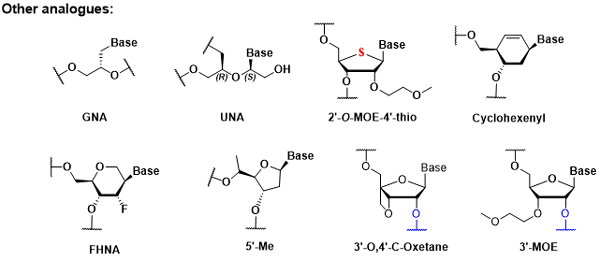
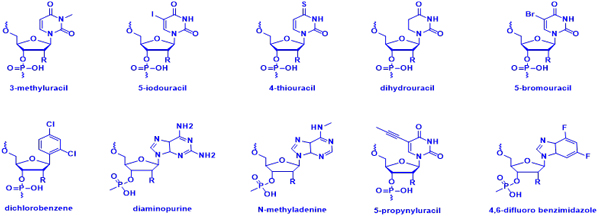
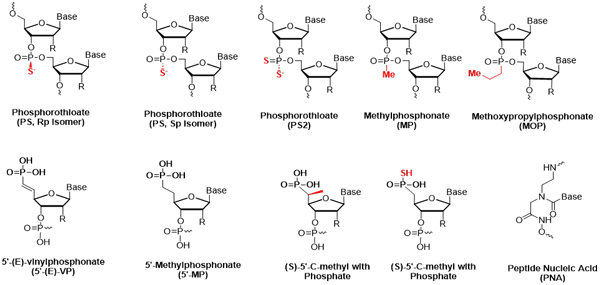
此外,美迪西具备多种核酸药物修饰技术,根据修饰位点的不同,可分为糖修饰、碱基修饰、骨架修饰以及递送系统修饰。这些修饰技术能够精准地针对核酸药物的特定部位进行改进,从而优化药物的稳定性、生物相容性和靶向性,为核酸药物的研发和应用提供强有力的技术支持。
美迪西在递送系统研发领域积累了丰富的经验,特别是在纳米颗粒载体(如LNP)和核酸偶联的GalNAc载体等方面,这些先进的递送技术确保了核酸药物在体内的高效递送。
脂质分子在人体内显示出免疫原性
未修饰的脂质不能被定向传递
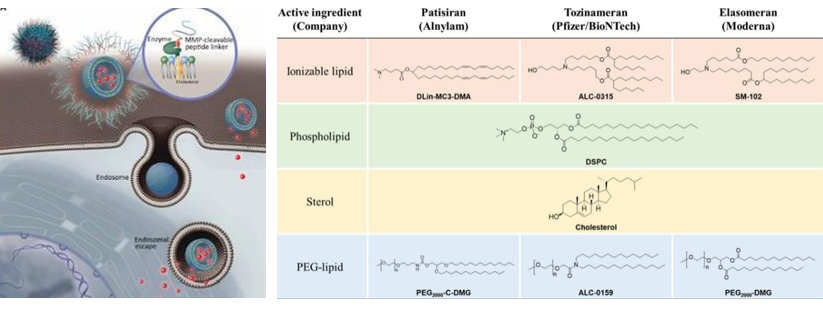
(1) lonizable lipid:
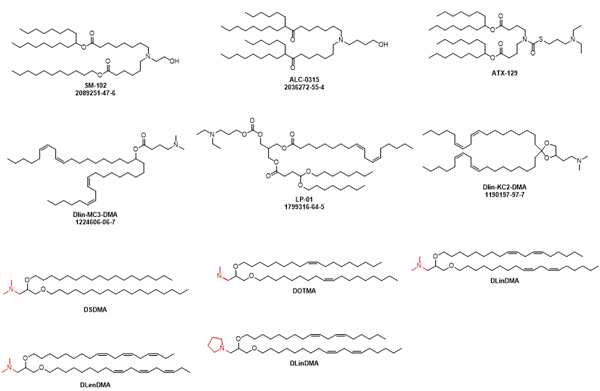
(2) Phospholipid:
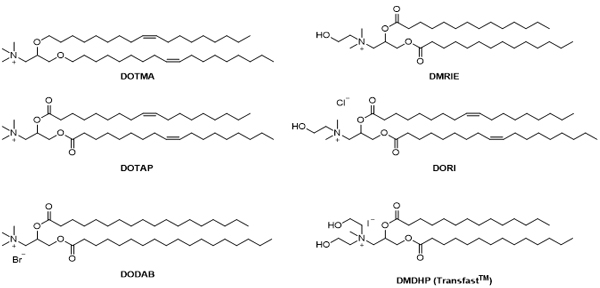
(3) Cholesterol series:
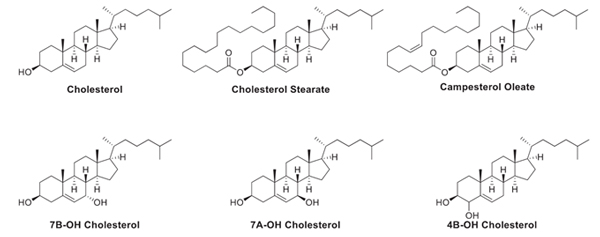
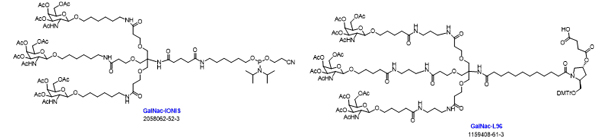
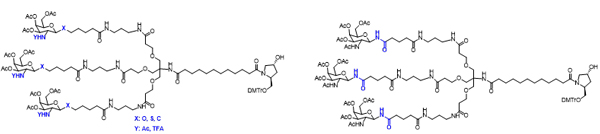
GalNAc不显示免疫原性,更安全
GalNAc的目标是肝细胞上的ASGPR,可以通过内吞作用被吸收
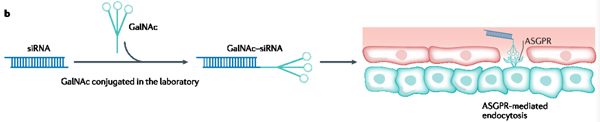
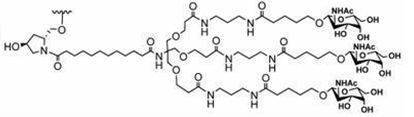
凭借健全的生物学分析能力,美迪西深入助力靶点表达分析、靶点序列分析、脱靶效应分析以及核苷酸序列设计,确保核酸药物研发的精准性和有效性。
美迪西拥有基于生物学的核酸药物筛选技术,涵盖体外筛选和脱靶效应评估:通过GaINAc和SiRNA结构优化,精确筛选和优化核酸药物的效能和特异性;深入研究脱靶效应,确保药物精准作用,保障安全性和有效性。
| GaINAc结构优化assay | SiRNA结构优化assay |
√ GaINAc-ASGPR1 binding assay-SPR,ELISA | √ psiCHECK2 luciferase reporter assay |
| 杂交依赖的脱靶效应 | 非杂交依赖的脱靶效应 |
√ psiCHECK2 luciferase reporter assay-seed sequence | √ TLR3/TLR7/TLR8 dependent cytokinerelease assay-PBMCs-ELISA/Luminex |
在评估核酸药物的递送效率时,生物分析方法的选择是不可或缺的步骤。这些方法涵盖了从传统的液相检测到针对细胞因子的分子检测等多种手段。然而,每种方法都有其独特的敏感性、差异性和潜在的局限性。其中,LC-MS/MS分析方法优先考虑。
| 方法 | 适宜的分析物 | 优点 | 不足 |
| qPCR(扩增后) | 非修饰的寡核苷酸(化学修饰可能会影响分析),不能过短,18个以上 | 高灵敏度,宽检测范围,通量能力中等至高水平 | 样品处理工作量大,低分辨率,低准确度,低精密度,特异性有限,易受基质干扰,不能区分原形和代谢产物 |
| 基于杂交原理但不扩增,如荧光标记探针,配体标记探针;抗体结合,ELISA | 修饰或未经修饰的寡核苷酸 | 特异性高(序列依赖性),宽检测范围,灵敏度好,准确度和可重复性良好 | 依赖探针、检测标记或抗体的可靠性,会受基质干扰,不能区分原形和代谢产物 |
| LC-UV/FL,色谱结合紫外检测(荧光检测) | 修饰或未经修饰的寡核苷酸,不能过短,24个以上 | 分开后呈现高的特异性,准确度好,宽检测范围 | 样品处理工作量大,灵敏度低,对分离要求高,若使用FL检测器,灵敏度依赖于荧光探针 |
| LC-MS/MS,LC-HRAM(TOF,Orbitrap等) | 修饰过的寡核苷酸,核苷酸不要过长,25个以下 | 对修饰后核酸特异性及灵敏度高,宽检测范围,灵敏度高,通量能力中等至高水平,准确度高,可重现性强 | 仪器昂贵,对非修饰核酸灵敏度及特异性差,对仪器损伤大 |
美迪西生物样品采集技术涵盖超声引导的肝脏活体取材、基于手术的肝脏活体取材、猴侧脑室给药以及经腰椎穿刺脑脊液采集等。这些专业技术的运用,为药物研发提供了至关重要的数据和资源支持。
| 类别 | 研究内容 | ASO | siRNA | |
| 种属选择 | 人和动物种属RNA结合的序列同源性分析,是否可呈现预期的生物学效应 | √ | √ | |
| 安全药理学 | hERG | √ | × | |
| 啮齿类动物FOB | √ | √ | ||
| 啮齿类动物呼吸系统安全药理研究 | √ | √ | ||
| 猴心血管呼吸系统影响研究(伴随在重复给药毒性试验中开展) | √ | √ | ||
| 单次给药毒性 | 啮齿类单次给药毒性试验(GLP或非GLP) | 多数不单独进行 | ||
| 猴单次给药毒性试验(GLP或非GLP) | ||||
| 重复给药毒性 | 啮齿类重复给药毒性试验(GLP) | √ | √ | |
| 猴重复给药毒性试验(GLP) | √ | √ | ||
| 免疫原性和免疫毒性 | 抗药物抗体筛查、滴度测定,必要时还要进行中和属性确定,免疫毒性(伴随重复给药) | √ | √ | |
| 遗传毒性 | 标准组合:Ames、染色体畸变和体内微核试验 | √ | √ | |
| 制剂安全性 | 体外家兔溶血+刺激性(可伴随在重复给药毒性试验中进行)+过敏性试验 | √ | √ | |
| 生殖毒性试验 | 生殖Ⅰ、Ⅱ、Ⅲ段试验(可在临床期间完成) | 适应症和用药人群 | ||
| 致癌性试验 | 根据证据权重法评估是否需要进行(转基因小鼠6个月和大鼠2年致癌性),可在NDA前进行 | √ | √ | |
| 发育毒性 | 幼龄动物给药试验 | 适应症和用药人群 | ||
| 类别 | 研究内容 | LNP递送 | 病毒载体 |
| 种属选择 | 表达蛋白及其靶点种属间同源性,是否可呈现预期的生物学效应,载体种属适用性 | √ | √ |
| 安全药理学 | hERG | √ | × |
| 啮齿类动物FOB | 取决于种属相关性 | ||
| 啮齿类动物呼吸系统安全药理研究 | 取决于种属相关性 | ||
| 猴心血管呼吸系统影响研究(伴随在重复给药毒性试验中开展) | √ | √ | |
| 单次给药毒性 | 啮齿类单次给药毒性试验(GLP或非GLP) | 多数不单独进行 | 单独进行价值明显 |
| 猴单次给药毒性试验(GLP或非GLP) | |||
| 重复给药毒性 | 啮齿类重复给药毒性试验(GLP) | 取决于种属相关性 | |
| 猴重复给药毒性试验(GLP) | √ | √ | |
| 免疫原性和免疫毒性 | 抗药物抗体筛查、滴度测定,必要时还要进行中和属性确定,免疫毒性(伴随重复给药) | √ | √ |
| 遗传毒性 | 标准组合:Ames、染色体畸变和体内微核试验 | √ | × |
| 制剂安全性 | 体外家兔溶血+刺激性(可伴随在重复给药毒性试验中进行)+过敏性试验 | √ | √ |
| 生殖毒性试验 | 生殖Ⅰ、Ⅱ、Ⅲ段试验(可在临床期间完成) | 适应症和用药人群 | |
| 致癌性试验 | 根据证据权重法评估是否需要进行(转基因小鼠6个月和大鼠2年致癌性),可在NDA前进行 | 适应症、用药频率 | |
| 发育毒性 | 幼龄动物给药试验 | 适应症和用药人群 | |
核酸药物的研发之路挑战重重,这些挑战无疑促进了行业内更广泛的合作与协同创新。为了进一步推动科研成果的转化,美迪西依托张江院士创新药熟化中心(GOI),与院士、教授等优秀科研人员展开了紧密的合作。这一合作模式不仅整合了各方优势资源,极大地促进了科研成果的转化效率,也促进了科研与产业的深度融合。同时,与优秀科研人员的紧密合作也使得美迪西能够紧跟国际科技前沿,不断提升自身的技术水平和创新能力。
持续探索与创新是科研的永恒追求,也是美迪西的核心动力与不懈追求。美迪西将不断深耕核酸药物等前沿研发领域,勇于突破技术壁垒,并积极寻求与优秀的科研机构和药企的广泛合作,助力更多具有突破性的药物早日走上临床。
美迪西核酸药物研发平台是集成了药物发现、生产和临床前研究的一体化综合性平台。基于严谨的科学态度、开放的技术平台和先进的仪器设备,我们可以满足行业对于前沿创新核酸药物的研发需求,承接医药公司及科研单位的核酸药物发现、筛选及临床前研究服务。
核酸药物合成&修饰:
美迪西核苷酸药物化学合成平台可以提供单体合成、修饰;寡核苷酸合成;递送系统合成以及寡核苷酸偶联物的合成。已经建成的siRNA库,不仅有丰富的单体库存,而且拥有庞大的单体合成砌块库,可以快速完成各类修饰单体的合成。美迪西拥有专业的小核酸药物的研发团队可以提供高效快捷地研发服务;已有多个siRNA药物FTE项目完成和进行中。
核酸药物CMC研究
在寡核苷酸药物开发过程中,药学方面的挑战主要是寡核苷酸大规模生产能力和分析与质控能力要求高,大规模生产对单体原料、设备、合成工艺及纯化方面都有很高要求。制剂方面的挑战在于制备LNP(GalNac技术的小核酸除外)的难度高;分析方面挑战在于寡核苷酸的有关物质与活性成分本身的结构相似性大,质量研究与控制需要多原理不同手段的分析方法进行,除了一般注射剂研究外还要进行LNP的包封率测定等。美迪西在siRNA等寡核苷酸药物方面的CMC服务项目已启动。
核酸药物药效学评价
在寡核苷酸药物开发过程中,药效学方面的挑战包括:靶向不足导致靶部位的寡核苷酸药物浓度低导致给药剂量不断增高;寡核苷酸药物与非靶 RNA 结合引发的脱靶毒性等。美迪西在核酸药物药效学评价方面经验丰富,提供不同用药途径的比较(如静脉注射,瘤内局部注射)、体内药效与靶标mRNA/蛋白质降解(PD)和寡核苷酸药物的系统暴露量(PK)的相关性分析等等。
核酸药物药代动力学研究
在寡核苷酸药物开发过程中,药代动力学PK方面的挑战也是此类药物较大的难题。未经修饰的寡核苷酸类药物成药性不佳、PK特性差、稳定性差、容易被核酸酶降解、分布特性差、和靶标的结合力不佳、生物分析方法开发难度大等。美迪西药代动力学团队具备完善的寡核苷酸生物分析平台、肝脏活体穿刺、肌肉活检和鞘内注射平台用于PK和PK/PD研究。
 相关新闻
相关新闻