
紧跟新药前沿,专注研发创新
本周看点
-
• 国内首个抗HER2抗体偶联物产品中国上市;
-
• 首款胆管癌靶向疗法口服抑制剂获批;
-
• 豪森宣布与Atomwise扩大AI战略合作;
获批上市
国内首个抗HER2抗体偶联物产品中国上市
近日,继帕妥珠单抗之后,罗氏又一重磅HER2阳性乳腺癌创新靶向药物恩美曲妥珠单抗近日正式中国上市,这距离1月20日恩美曲妥珠单抗获得国家药品监督管理总局批准用于紫杉烷类联合曲妥珠单抗为基础的新辅助治疗后仍残存侵袭性病灶的HER2阳性早期乳腺癌患者仅短短三个月。
据悉,作为全球首个获批的单药治疗实体瘤的抗体药物偶联物(ADC),也是首个登陆中国的抗体偶联物(ADC)类里程碑式的靶向抗癌药物,恩美曲妥珠单抗全新的作用机制将使新辅助治疗后仍残存病灶的HER2阳性早期乳腺癌患者复发或死亡风险降低50% ,这将为高危复发风险HER2阳性早期乳腺癌患者带来全新的治疗选择。
Incyte公司FGFR口服抑制剂获得FDA批准
2020年4月18日,美国食品药品监督管理局(FDA)加速批准了美国Incyte公司研发的Pemazyre(pemigatinib)用于治疗经治晚期胆管癌成年患者。这是全球首款胆管癌靶向疗法。
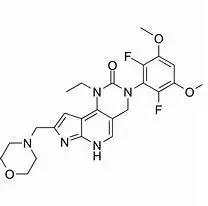
pemigatinib
胆管癌是在将消化液从肝脏运送到胆囊和小肠的细长胆管里发生的一种罕见癌症。在诊断时,大多数胆管癌患者已经为晚期,这意味着他们无法接受手术治疗。对于这些患者,化疗组合药物已成为标准的初始治疗方法。约9%至14%的胆管癌患者的肿瘤中发现了纤维细胞生长因子受体2(FGFR2)融合。今天的批准适用于局部晚期或转移性的的胆管癌患者,这些患者的肿瘤具有FGFR2基因融合或其它重排。Pemazyre片剂通过抑制肿瘤细胞中的FGFR2而阻止肿瘤的生长和扩散。
融资
Avectas细胞工程平台完成2000万美元C轮融资准
最近,Avectas是一家总部位于爱尔兰的细胞工程技术平台,已完成了一笔约为2000万美元的新的重要C轮新股权融资,迄今为止,对该业务的总股权投资已达4,000万美元。本轮融资由现有股东牵头,其中包括经验丰富的生物制药公司高管Seamus Mulligan。
在最新一轮股权融资中筹集的资金将用于加速Avectas专有细胞工程技术平台(Solupore®)的临床转化和商业推广。为了支持下一阶段的活动,在与Covid-19相关的条件允许的情况下,Avectas还将在爱尔兰和美国聘用新员工来扩展其商业,法规和技术组织。
Immunovant完成约1.4亿美元再融资,加速FcRn抗体临床开发准
2020年4月16日,Immunovant,Inc.(纳斯达克股票代码:IMVT)是一家临床阶段的生物制药公司,致力于为自身免疫性疾病患者提供正常生活,宣布已完成其先前宣布的承销公开发售的9,613,365股普通股,其中包括全部行使承销商的选择权,以每股14.50美元的价格购买1,253,917股普通股。从此次发行中,Immunovant的总收益总额约为1.394亿美元,其中不包括承销折扣和佣金以及发行费用。所有普通股均由Immunovant出售。

Immunovant候选研究产品IMVT-1401(以前称为RVT-1401)是一种针对新生儿Fc受体(FcRn)的新型完全人源的单克隆抗体。该产品具有通过皮下注射解决多种IgG介导的自身免疫疾病的潜力。
合作
豪森和Atomwise宣布扩大AI战略合作
近日,中国领先的生物制药公司豪森药业(HK:3692)和用于药物发现的人工智能(AI)的领导者Atomwise宣布扩大与AI加速药物发现的战略伙伴关系。在完成首次发现合作之后,该合作伙伴关系立即扩大,该合作仅在4个月内就成功鉴定并实验确认了多种新颖的化合物,以实现以前具有挑战性的肿瘤学靶点。

利奥制药5.7亿美元引进台湾合一生技FB825全球权益
2020年4月15日,LEO Pharma(利奥制药)宣布与Oneness Biotech(合一生技)和Microbio Shanghai(中天上海)达成一项协议,该协议涉及治疗特应性皮炎和过敏性哮喘的实验药物FB825的全球开发和商业化。根据协议,LEO Pharma将支付4000万美元的预付款,其中Oneness和Microbio Shanghai有资格获得最高5.3亿美元的里程碑付款,其次是高单位数到两位数的特许权使用费。
关于美迪西
美迪西(股票代码:688202)是一家药物研发外包服务公司(CRO)。成立于2004年2月2日,公司走过16个年头,在上海建立了一家集化合物合成、化合物活性筛选、结构生物学、药效学评价、药代动力学评价、毒理学评价、制剂研究和新药注册为一体的符合国际标准的综合技术服务平台,并得到了国际药品管理部门的认可。美迪西普亚的动物实验设施获得AAALAC(国际动物评估与认证协会)认证和国家药品监督管理局NMPA GLP证书,并已达到美国食品药品管理局GLP标准。
美迪西拥有丰富的全球合作经验,2015年以来,美迪西在全球服务超过500家活跃客户,已为武田制药、强生制药、葛兰素史克、罗氏制药等多家全球性制药公司及恒瑞医药、扬子江药业、石药集团、华海药业、众生药业等国内外知名客户提供研发外包服务。
联系我们
Email: marketing@medicilon.com.cn
电话: +86 (21) 5859-1500(总机)








 相关新闻
相关新闻