从近年来的创新药研发和销售市场来看,生物药占尽风头,小分子药物由于作用机理的种种局限,无法作用于所有的药物靶点而日渐式微。
PROTAC的问世为解决小分子药物的这一局限带来了极大的潜力,为靶向传统小分子药物所不可成药的靶点带来了解决方案。
2017年以后,PROTAC技术飞速发展,从实验室走向工业界,从Harvard大学,Yale大学开始, Arvinas公司, C4公司, Kymera Therapeutics公司相继成立专门从事PROTAC技术药物研究,得到约20亿美元的资金,药物研发巨头均纷纷加入该行列,包括辉瑞,罗氏,GSK,默克,诺华,默沙东、艾伯维、吉利德、百时美施贵宝等。
2019年3月,Arvinas公司宣布其开发的用于治疗前列腺癌的雄激素受体(AR)降解剂ARV-110进入Ⅰ期临床试验,这是公开报道的第一个进入Ⅰ期临床试验的PROTAC分子,标志着PROTAC技术的研究进入新的阶段。
3月13日美迪西化学部副总裁马兴泉博士在“美迪西云讲堂”与各界同仁们分享了关于PROTAC技术的精彩讲解,下文对马博士的课程做了简单的回顾,各位可以扫描下方二维码或点击文末的“阅读原文”,进入视频回放链接,观看完整视频!
01 小分子药物的瓶颈
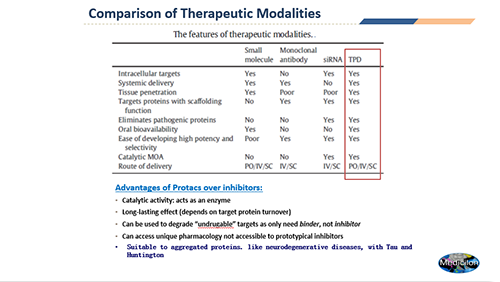
传统的小分子抑制剂的作用机制是通过结合靶蛋白的活性位点从而抑制靶蛋白的功能,100多年来小分子的研发思路成功对抗了很多疾病。但小分子成药的技术也面临着诸多的限制和挑战,例如小分子药物会出现耐药性,无法长期抑制靶向蛋白的活性;且小分子药物需要维持一定的体内药物浓度才能发挥作用;另外,还有很多靶点被认为是小分子所无法靶向的,如一些转录因子,骨架蛋白和无药可治的突变靶点KRAS等。
单抗虽然相对于小分子具有高亲和力和高选择性的优势,但其最大弊端在于无法透过细胞膜,因此无法作用于细胞内靶点。RNAi可以透过细胞膜,并对靶点有强作用力,然而由于其代谢不稳定及脱靶效应等弊端,发展进程也是困难重重。
然而
PROTAC技术的出现给小分子药物的瓶颈带来了曙光,似乎可以完美地解决小分子药物面临的诸多难题。
02 神奇的小分子药物技术-PROTAC
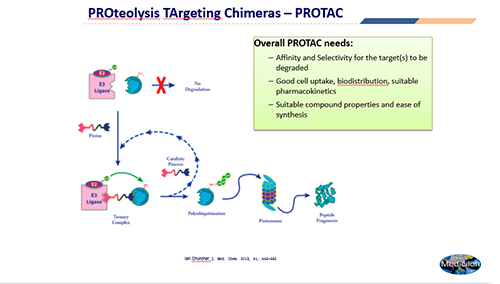
PROTAC是PROteolysis TArgeting Chimeras的缩写,意为蛋白水解靶向嵌合体,属于蛋白质降解技术的一个新分支。PROTAC技术的原理征用了自然的细胞内蛋白质降解过程。蛋白降解在细胞的正常生命活动中是至关重要且被严格调控的,其过程主要是通过泛素化酶系统的参与而完成的。需要被分解的蛋白质通过E1、E2和E3泛素连接酶系统标记,进而被蛋白酶识别并降解。
PROTAC分子是一类具有哑铃型结构的双功能活性化合物,分子的一个活性端可以与靶蛋白紧密结合,并通过连接链linker连接到另一个活性端用来与E3泛素连接酶相结合。这种双功能分子在体内可以分别识别靶蛋白和E3泛素连接酶,将靶蛋白和E3泛素连接酶拉近,靶蛋白被泛素化后,在体内通过泛素-蛋白酶体途径降解。靶蛋白降解后,PROTAC分子又可以被释放出来参与到下一个蛋白的降解过程,因此这种降解作用具有催化效果,较少的药物剂量就可以实现高效的降解。
03 PROTAC技术的发展历程
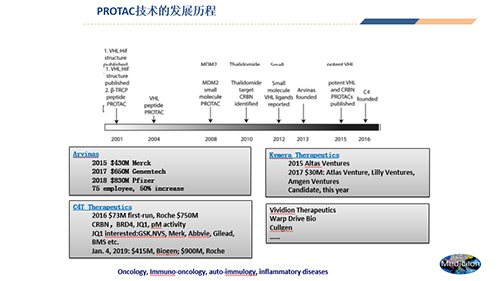
2001年加州理工大学的Raymond J. Deshaies教授和耶鲁大学的Craig M. Crews教授首次提出了PROTAC的概念,他们报道了利用一段肽段与小分子的连接物可以人为调控目的蛋白的表达水平。2004年,Crews和Alessio Ciulli等人设计并改造了VHL(E3泛素连接酶复合物CRL2VHL的一部分)的配体,获得了具有高亲和力的VHL的配体,与VHL的结合力可以达到纳摩尔级别。利用这种小分子配体,Crews课题组于2015年报道了雌激素相关受体α(ERRα)和RIPK2 的PROTAC分子,都可以在细胞水平观察到靶蛋白的降解。Crews教授在2013年建立了Arvinas,公司使用PROTAC平台构建广泛的蛋白质降解产物候选管道,以针对各种器官系统和组织中的疾病,是PROTAC分子发展的龙头公司,目前ARV-110和ARV-471推进到 I 期临床试验中。
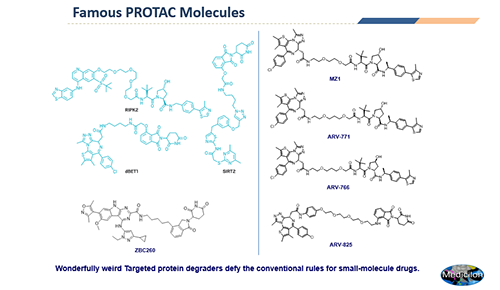
04 PROTAC研究中的要素
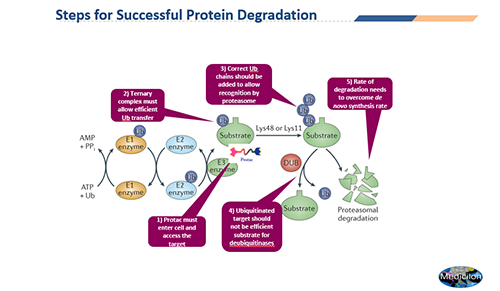
PROTAC发挥药效必须与靶蛋白和E3酶形成有效的三元复合物,而此过程对PROTAC来说,首先需要成功的通过细胞膜进入细胞,其次要考虑如何控制浓度以避免药物分子与靶蛋白和E3酶分别形成二元复合物(hook effect),以及充分考虑靶蛋白与E3酶接触区域的电荷排斥和立体结构排斥,显得非常重要。而当三元复合物形成后,能否有效降解,还需要与去泛素化酶以及靶蛋白重合成作斗争,直到达成一定程度的平衡。
其次,E3泛素连接酶的选择也尤为关键。已知大约有600个E3泛素连接酶可以调控蛋白酶体的功能,这就为蛋白质靶向治疗提供了无限机会。由于靶向蛋白降解的整个过程依赖于配体诱导的接近性,因此E3泛素连接酶与靶蛋白在时空上的共定位是至关重要的,组织表达、亚细胞定位和调控的差异都可能带来潜在的陷阱和机会。
除了重新利用不同连接酶存在的生物学差异外,目前可用的连接酶之间还存在着一些物理化学方面的差异,如何获得合适的物理化学性质以及吸收、分布、代谢和排泄(ADME)特性,使之足以口服给药和/或甚至达到中枢神经系统是极其重要的。
05 美迪西PROTAC研究平台
美迪西科研团队建立了PROTAC药物发现技术平台,汇总了当前流行的热门的靶标蛋白配体, 建立了广泛的热门靶向蛋白高度亲和力小分子及小分子片段化合物库(TPSM),广泛的E3连接酶高度亲和力的小分子及小分子片段(E3SM);建立了linker系统,包括收集大量具有广泛多样性的双官能团连接体(BF-Linker)。这些积累的化合物库可以帮助快速高效的合成大量高活性PTROTAC双特异性小分子,极大地提高采用PROTAC技术进行的药物研发过程。除了快速合成之外,我们同时建立和完善的PROTAC生物筛选与测试平台,后续发展到临床前所有阶段。我们的目标是建立起的技术平台能同时承担10到20个PROTACT研发项目,每年能帮助产生10到20个PROTAC候选药物。
美迪西的PROTAC研究平台已经与多家生物医药公司建立了技术服务,部分项目已经推进到临床前研究阶段。“专注创新,用心服务”,经过不断创新和完善,美迪西PROTAC研究平台已有能力进一步承接大量的PROTAC技术研究,提供一站式的研发服务。

THE END
往期精彩回顾
美迪西云讲堂第01讲:
美迪西云讲堂第02讲:
美迪西云讲堂第03讲:
美迪西云讲堂第04讲:
美迪西云讲堂第05讲:









