近日,美迪西CMC主任周晓堂上海2019药品研发管理高层论坛培训班上做了《药物研发思路》专题演讲,下文是演讲内容的主要摘要,由美迪西编辑整理,以飨读者。

美迪西CMC主任 周晓堂
QbD(Quality by Design)的概念最早是在2004年由美国FDA提出的,并被纳入到ICH质量体系当中成为指导原则和指南。QbD,即质量源于设计,是指药物的质量控制应该从最早期的研发设计环节做起。与之前的QbT(Quality by Test), QbP(Quality by Product)相比,进一步向前推进了质量控制包括的环节,为整个过程可以更加充分、科学的研究和开展奠定基础,使新开发的药物能够更加顺利的通过检验。设计空间(Design Space)是一个与之相伴随的概念,指的是药品质量(如溶解度等)与多个生产条件要素参数之间的多维度函数,在此函数中符合药品质量要求的区域被称为设计空间,其意义在于之后的研发和生产操作都应在此空间之内,一旦超出则视为变更,需要重新评估调控。(见图1)
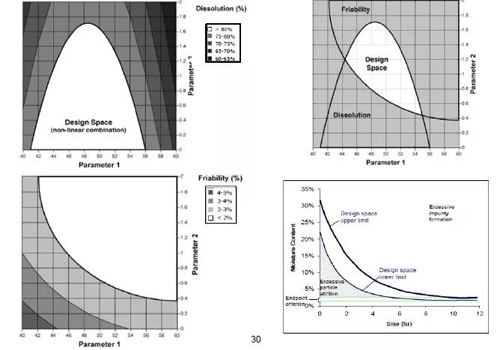
(图1 设计空间函数曲线)
图中的横纵坐标代表了生产条件的两个重要参数,图中白色的设计空间即可理解为在设计中符合预期标准的空间。在这个空间内任何条件的组合都被认为是符合预期质量控制的。
设计空间的概念主要在ICH的Q8指导原则中有详细介绍。Q8、Q9和Q10三个指导原则是ICH在2005年和2008年发布的三个关于质量控制和质量实施工作的指导原则,清晰地解释了QbD原则及其在整个过程中的各方面应用。Q8(药物研发)、Q9(质量风险管理),和Q10(药物质量系统),是三大贯穿于从处方开发、工艺开发到生产整个药物生命周期的指导法规,共同发挥作用促进产品的质量系统。其中,Q8(R2)法规中包括了目标产品质量概况(QTPP)和设计空间(DS)的建立和潜在的关键质量属性(CQAs)的确定;Q9法规包括了产品开发过程中的风险评估(QRM),建立控制策略时的风险控制和产品质量持续提升中的风险回顾;Q10主要阐述了药物质量系统(PQS),包括了工艺性能和产品质量监测系统、CAPA系统、变更管理系统和管理回顾。值得强调的是,三个指导法规是共同,在产品的整个生命周期中发挥作用,将QbD的研发理念付之于实践的指导原则当中。
那么引入QbD概念的意义在哪里呢?从环节上看,它加入了更前端的环节,增加了工作量。然而深入QbD的研发方案所带来的优势也是显而易见的,因为设计对工艺验证的控制,使得注册的成本降低;加上对产品持续性的质量控制和系统调控,使得产品上市后变更少,不确定性和风险性降低,整体上降低了失败的概率。同时,QbD的实验方案带来了对工艺更深刻的理解,技术应用和工艺分析的加强,注册和药政标准全球化,研发效率提升,最后带来的是产品质量的全面提升。所以从全局来看,QbD极大的提高了研发效率,节约了成本,增加了可控性。QbD起始于研发最开始的阶段,并贯穿于发展的各个阶段和过程,与摸索的阶段性结果相结合并提出改进,实现了质量把控的持续更新,螺旋上升。
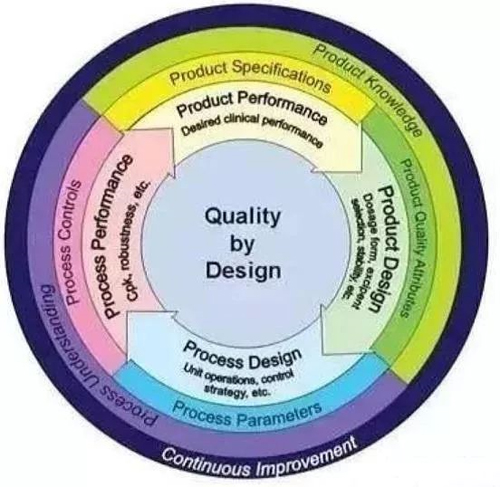
(图2 QbD的螺旋上升结构)
QbD的理念不是一个步骤,不是前期做好之后就可以一劳永逸的。药品设计,工艺设计,工艺优化和产品优化四个环节一环扣一环,在研发过程中周而复始不断循环,螺旋上升,不断改良。
在应用方面,QbD理念可以实践于广阔的研发和注册领域。体现QbD理念的Q8、Q9、Q10三大指南对于所有的的产品,产品开发方法和注册申报均有指导意义,包括但不局限于新药、仿制药和已上市的药品;简单和复杂剂型;小分子和生物技术产品;传统研发和QbD研发;ICH管辖的领域及非管辖领域。下面我们就仿制药和创新药为例,来对QbD理念的应用来详细举例。
QbD药物研发在面对仿制药和创新药时有着显著的差异。仿制药的研究因为有参比制剂做标准,所以其研发思路和目标都是围绕参比制剂的。与参比制剂的一致性以及优于参比制剂,是
仿制药研发的核心目标。仿制药研发流程主要包括以下几个模块:处方前研究,处方工艺研究,工艺放大,工艺验证和上市申请。仿制药的处方前研究,包括原辅料性质研究,原辅料相容性研究和参比制剂研究以及反向工程。在仿制药研究中,常用到的思路是反向工程,即将参比制剂的处方进行拆解和分析,比如用XRPD、NMR等方法对原研药的API晶型进行解析,通过EMA说明书来分析参比制剂的辅料种类和用料等等,来对参比制剂的原料、处方和制备工艺进行解析,并作为仿制药研发的标准。
创新药研发是一个从无到有,摸索前进的过程,因此创新药的研发具有渐进性和不确定性,主要包括处方前研究,处方工艺研究,临床前研究,临床研究I、II&III期研究以及新药NDA申报。在探索研发的过程中,存在着许多不确定性,在不同的阶段下研究目的的侧重点也不相同,例如在临床I期研究阶段,着重关注药物的安全性,而在临床III期除了研究关键批次的安全性外,还要以有效性作为目的来考察。同时由于其不确定性,导致创新药研发过程中常常会涉及到变更,而在临床III期时的变更风险相对来说比较大,可能会对药物的安全性或体内行为产生影响,因此需要进行风险评估并进行适当的桥接研究。
在创新药摸索的道路上,美迪西生物医药是很好的助力,美迪西拥有十几年参与药物研发,探索创新药的经验,积累了几十例与国内外大企业共同研发的成功案例,对于QbD的理念有着深刻的认识并认真付诸于实践和每位科研人员的日常工作中。同时,美迪西生物医药在仿制药的研发上也有着丰富的经验和严谨规范的团队,为研发和注册申报的成功保驾护航。

美迪西工艺与放大服务

美迪西制剂服务
美迪西是一家药物研发外包服务公司(CRO),在上海建立了一家集化合物合成、化合物活性筛选、结构生物学、药效学评价、药代动力学评价、毒理学评价、制剂研究和新药注册为一体的符合国际标准的综合技术服务平台,并得到了国际药品管理部门的认可。美迪西普亚的动物实验设施获得AAALAC(国际动物评估与认证协会)认证和中国食品药品监督管理局GLP证书,并已达到美国食品药品管理局GLP标准。美迪西以高效、高性价比的一站式专业服务帮助客户更快地达到目标。
联系我们:
电话: +86 (21) 5859-1500(总机)









 相关新闻
相关新闻