




在刚刚闭幕的全国人大代表大会上,不少医卫界代表、委员纷纷提出了有关眼底疾病的建议和话题。无独有偶,去年颁布的“十四五”全国眼健康规划(2021-2025年)中眼底病首次被提上国家战略,将眼健康作为提高国民健康水平的重点工作内容。
我国眼健康现况确实严峻,中国是全球眼病患者最多的国家。随着我国老龄化趋势的发展,白内障、青光眼、干眼症的患病人数呈现上升趋势,由高血压、高血糖引发的视网膜病变患者年龄也在逐渐年轻化。近视是最常见的眼部疾病,目前我国近视患者人数已超6亿人,近视率高达48.5%,而且青少年近视率甚至过半[1]。

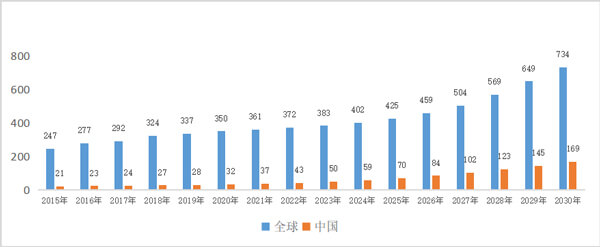
面对持续走热的眼科话题,我国的眼科药物发展迅猛,但依然还无法满足市场的需求。根据资料显示,中国眼科药物市场规模自2015年的21亿美元增长至2019年的28亿美元,复合年增长率为8%,远超全球的复合增长率,国内眼科药物的复合增长率还会持续增长,预计在2030年到达19.1%,国内眼科药物市场规模达到169亿美元[2]。
为了尽快填补市场对眼科药物的需求,近年来眼科药物持续获批,越来越多的药企加入到眼科药物的研发和生产中。根据药融云数据库显示,2014年至今,中国共有234个眼科新药,其中处于药物发现阶段的药品共有15个,处于临床前阶段的药品数量为61个,临床阶段而言,II期临床的产品最多,达到47个。
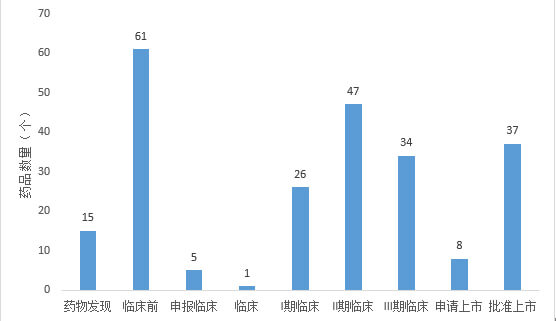
中国眼科新药研发阶段药物数量(2014年-2022年9月14日)[3]
但由于眼科疾病相关基础研究进展缓慢,关于药物的研发,中国主要集中在开发已获批药物的改良工艺或剂型上。眼科疾病药物主要剂型分为:滴眼剂、注射剂、凝胶剂、眼膏剂、片剂药五大类,其中,滴眼剂长期主导着眼科市场,品类繁多。

美迪西眼科药物制剂服务涵盖滴眼剂、注射剂、凝胶剂、眼膏剂四大类型,完成多款滴眼剂和玻璃体注射新药的制剂安全性研究并助力获批临床。
注射剂眼科药物由于其给药方式难度大在研发阶段遇到的阻碍比其他剂型大,美迪西的临床前眼科研究平台可以实现对兔、狗、小型猪及非人灵长类等动物种属实现独特的精细给药,包括:视网膜下腔注射、脉络膜上腔注射、玻璃体腔注射等,利用多年的丰富实践经验和先进设备,解决客户关于眼科研究的各种复杂问题,专注细节,把控质量,为客户提供稳定优质的研究服务。
VEGF是眼科类药物开发研究得最多的靶点,抗VEGF药物能够减少新生血管形成,降低血管通透性。在全球眼科药物市场,由于抗 VEGF 药物能有效抑制新生血管的形成并促进已有的新生血管消退,其已成为湿性年龄相关性黄斑变性(wet-AMD)、糖尿病视网膜病变(DR)、糖尿病黄斑水肿(DME)和视网膜静脉阻塞 (RVO)等眼底血管疾病的一线疗法。
不管全球还是中国,抗VEGF眼科药物的研发赛道市场竞争非常激烈。据药融云眼科行业白皮书统计,包含批准上市的,全球范围内有105个,中国有24个。
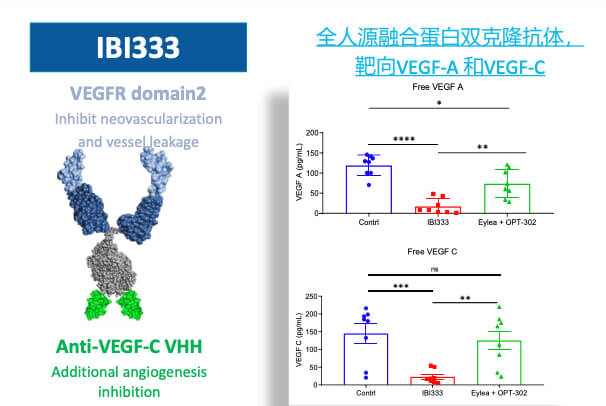
图片来自:信达生物
2022年9月19日,信达生物自研产品抗VEGF-A/VEGF-C双特异性抗体IBI333在国内获批临床,适应症为新生血管性年龄相关性黄斑变性(nAMD)。这也是全球首款获批临床的抗VEGF-A/VEGF-C双抗。
同时,信达生物管线中还有2款抗VEGFR眼科药物已进入临床阶段,分别是IBI324(抗VEGF/Ang2双抗)、IBI302(VEGF/Complement),在国内VEGF靶点赛道上处于领跑位置[4]。
遗传性视网膜疾病(IRDs)由于大多数导致疾病的基因突变已经被确认,因此基因治疗中进展最迅速的适应症领域就是眼科。
其中,以AAV病毒载体为主要应用模式。临床试验表明,在眼睛中使用腺相关病毒(AAV)载体递送基因疗法能够达到治疗多种遗传性眼病的效果且不会引起显著的免疫反应和全身性副作用。
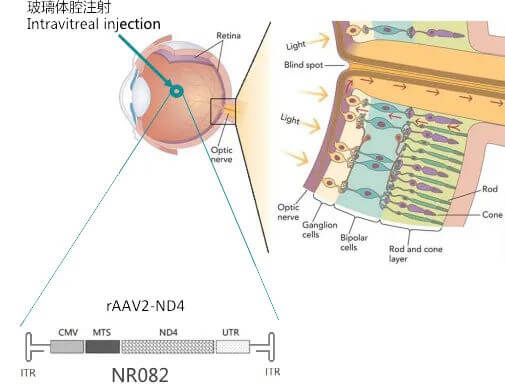
图片来自:纽福斯生物
2017年12月,眼科用药市场诞生了第一个基因疗法——Spark研发的Luxturna获批上市。三年后,首个中国自主开发的体内基因治疗产品——纽福斯研发的NR082(rAAV2-ND4)获得美国FDA孤儿药认证,并在2021年3月在国内获批开展临床试验。
据最新消息,今年2月22日,NR082在中国已完成III期临床试验的全部患者入组给药,期待首个基因治疗眼科药物在中国早日上市[5]!
为了更好地助力行业发展,美迪西将联合眼科药物相关企业于2023年04月07日开展眼科药物线上论坛上半场,展开眼科药物研发及应用的激烈讨论,欢迎各位医药同仁参与观看,还有惊喜好礼相赠!



[1] https://new.qq.com/rain/a/20230308A0A81900
[2] https://www.163.com/dy/article/FG7Q3ILF0519D8QI.html
[3] https://www.pharnexcloud.com/zixun/sd_5239
[4] http://cn.innoventbio.com/#/pline
[5] https://www.neurophth.com/ProjectD-17.html