



2023年3月4日,科镁信生物联合创始人&副总裁张翼博士在基因治疗闭门研讨会—美迪西核酸药物研发专场中做了主题为《阳离子脂质高通量定制化筛选》的报告,本文根据专家报告内容整理,并经专家审核确认。

嘉宾简介
张 翼 博士
科镁信生物联合创始人&副总裁
2021年回国,联合发起创立科镁信生物,担任副总裁,负责公司战略规划,领导开发非病毒基因递送平台。
张博士在Translate Bio(现赛诺菲)、Codiak和Beam therapeutics拥有10年的药物递送经验,专注于核酸疗法递送技术。在他的整个职业生涯中,他致力于开发用于各种核酸治疗的LNP输送平台。在Translate Bio和Beam Therapeutics,他是脂质发现团队的领先科学家,并发表了15项关于新型阳离子脂质的专利。他在三个mRNA LNP IND中发挥了关键作用,并推进至临床。在科迪亚克,他领导了外泌体和核酸纯化的工作。
张博士在复旦大学获得高分子科学理学士学位,在德克萨斯大学达拉斯西南医学中心获得生物工程博士学位,在麻省理工学院和康奈尔大学接受了4年的药物递送博士后培训。
核酸药物最大的问题就是稳定性问题,我们知道RNA药物是一个中间体,不稳定性是其与生俱来的一个缺点,也是生物进化当中对生命健康的一种保护。那如果要把一个不稳定的RNA这样一个中间体做成药的话,那么一个有效的保护体系就是非常重要的。核酸药物可以大体上分为小核酸和大核酸两种,第一个被批准的siRNA药物其实是用LNP来递送的,但后来发现,小核酸是可以通过化学合成的,它的主链可以通过化学修饰而变得更稳定。LNP就不是一个必要的起到保护作用的递送载体。但是对于mRNA或者其他的大核酸来说,化学修饰就不是一个可行的选择,因为mRNA主链不能进行任何的修饰,它的不稳定性是与生俱来的。那么LNP对大核酸来说还是非常重要的一个递送载体。
目前LNP临床阶段已验证的应用主要有被批准的Onpattro(siRNA)以及针对COVID-19的mRNA疫苗,同时在各管线产品中还有一些拓展应用,如CRISPR/Cas基因敲除、基因编辑/基因敲入、RNA编辑、环状RNA、体内Car-T和肿瘤疫苗。
但是其实所有潜在的核酸药物,包括siRNA和mRNA,以及DNA都是LNP可递送的潜在对象,只要带正电,LNP就能对它进行有效包裹和递送。
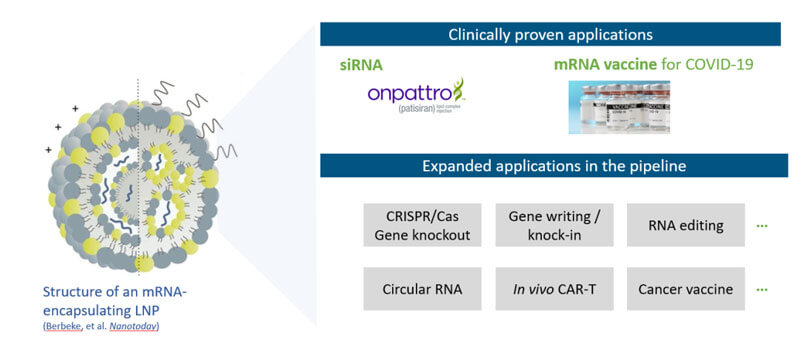
图1 LNP的结构及其应用
我们人体的一些疾病是由于蛋白翻译不正常造成的,不管是过高还是过低,我们都可以通过这个RNA药物来对它进行治疗。所以这个应用场景是非常广泛的。不同的核酸不同的给药方式以及不同的靶向性等这些因素是要靠我们的递送系统来实现的。第一步就是要把核酸药物准确地、高效地递送到病灶,从而对疾病进行治疗。现在有越来越多的证据证明,LNP可以有效地把核酸药物递送到不同的组织、不同的器官。
那大家对现在对这个阳离子脂质的重要性和价值的认识也越来越多,有很多工厂和一些新兴的公司,都会采取一个对外合作或者收购的形式去弥补其在LNP这一块的缺失。在当下LNP研发环境中,还是有一些挑战和机遇,可以说挑战和机遇是共存的。其中两个是很重要的,第一个是我们要有自有专利的阳离子脂质,具有全球FTO和独占性,就是我们常说的被卡脖子的一个技术环节。第二个是我们一定要找到适合不同应用场景的LNP来满足不同的组织靶向性,从不同的给药途径来做出适合不同应用条件的基因治疗表。
其实从2000年时,大家就已经对LNP进行研发了,可直到2020年,由于新冠,我们才有了第一个LNP作为递送系统的mRNA药物被批准。相对来说,这个发展还是比较缓慢。那制约LNP发展的因素主要有以下三方面因素,不同的制约因素也决定了我们采用不同的策略。
我们知道,阳离子脂质的结构对于LNP的递送效率是至关重要的。大家也在尝试设计不同结构的阳离子脂质,但是到目前为止,大家都没能建立一个有效的构效关系。我们不知道怎样结构的阳离子脂质具有高效的递送效率,具有特殊的靶向性。为解决这个问题,我们采取网筛的策略。也就是说,如果我们筛100个,筛不到,那我们就筛200个、500个,甚至1000个,直到筛到我们想要的结构。简言之,就是我们筛得越多、越快,就会有更高的机率得到一个我们想要的阳离子脂质。
我们在细胞实验上,比如筛选出比较好的阳离子,就可以把它放到动物体内去做表征的时候,发现这个药效完全是一个相反的结果。细胞实验非常好,然后动物实验当中没有任何蛋白表达。也就是说,在LNP的研发过程当中,我们没有办法使用传统的高通量、低成本的细胞实验对其进行一个预筛选,那我们只能在这个低通量和高成本的动物实验上对它进行表征。
前面提到LNP的应用场景有很多不同的核酸载荷、不同的给药方式。也就是说,每一种应用场景其实对LNP都有一个特殊的需求。我们发现不同的核酸、不同的给药方式,对不同的LNP有不同偏好。这就使得我们要去对LNP进行一个定制化的开发,让它适合不同的应用场景。
基于这三个因素,我们觉得传统研发思路不适用于LNP。理想的LNP研发平台需要满足以下几点:
1. 强大的阳离子脂质库;
2. 高通量体内筛选;
3. 针对载荷、靶点以及给药方式的定制化开发。
其中三大核心能力主要体现在:
我们设计新型脂质骨架结构,月产出100-1000种高纯度阳离子脂质体来进行内部高通量筛选,并且围绕新型脂质体结构申报具有全球技术壁垒的知识产权。
可应用于递送效率以及不同组织靶向性的动物水平的高通量筛选平台,可以进行高效筛选通量可达每日上百种LNP,且有效节约成本。
我们针对不同脂质体结构开发最优制剂工艺,采用新型生产工艺赋予LNP特殊功能,利用坚实的工艺放大生产产业经验。
这三大核心能力需要解决的事情、实现的目标有两个:更高递送效率、更好耐受性的肝靶向阳离子脂质;具有高效肝外靶向的阳离子脂质。
我们这样LNP筛选平台能够帮助我们去解决到一些传统研发手段所不能解决的问题。这个筛选的起点都是从我们具有自主知识产权的阳离子脂质库开始的。我们会对所有合成出来的阳离子脂质,通过静脉给药的方式,进行一个体内药效的初筛,得到高药效脂质。然后我们再会把这部分筛选出来阳离子脂质,在动物实验上进行进一步的筛选。比如,除了静脉给药方式,我们也会考察其他的给药方式,看不同LNP适合哪种给药方式,我们同样也会从核酸载荷和靶向性方面进行定制化筛选。然后我们还将这些LNP进行进一步的耐受性筛选。最终筛选到的少数LNP被认为是药效高、耐受性好的LNP。(如图2)
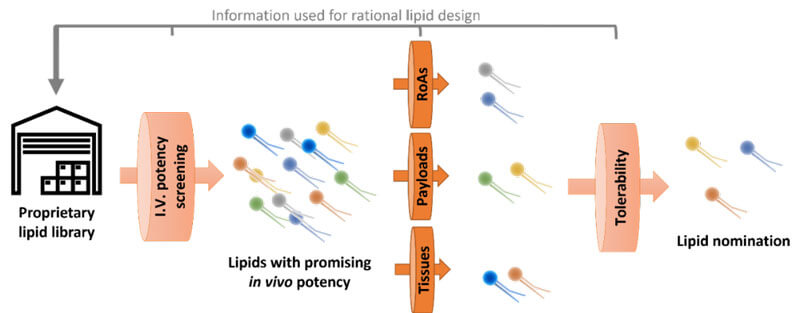
图2 科镁信LNP筛选流程
通过设计并筛选“成千上万”个阳离子脂质,我们能:
1.根据不同应用定制LNP;
2.拓宽新的专利空间;
3.加快建立基于大数据分析得到的构效关系,从而指导阳离子脂质结构设计。
接下来,张翼博士还分享了科镁信LNP高通量筛选平台取得的一些进展。首先是高通量合成和筛选方面,在过去的半年多时间内,我们已经合成并筛选了700个自主知识产权的阳离子脂质,并希望在今年年底,这个数量能够达到2500个,筛的更多,筛的更快,从而得到更好的阳离子脂质结构。
同时我们也评估了这些我们设计出来的阳离子脂质的体内核酸递送效率,找到了有80个阳离子脂质,表现出了比MC3 LNP更高的蛋白表达效率,其中有两个LNP是达到十倍的翻译效率。那我会把这80个LNP放到其他的应用场景上,进行进一步的筛选。那我们针对这80个LNP当中挑选出适合不同应用场景的LNP,即进行定制化筛选。比如适合静脉给药的CPL-180和CPL-092, 适合肌肉给药的CPL-457, 适合基因编辑工具的CPL-455,以及适合靶向T细胞的CPL-180等。
除了阳离子脂质筛选呢,我们也会利用我们独特的工艺开发优势解决LNP目前的一些短板。
1. 第一个优势就是解决耐受性问题。我们知道阳离子脂质是作为一个带正电的小分子,它的生物安全性、耐受性始终是被大家诟病了一个地方。大家采取一个策略就是不断的降低它的剂量来去减缓这个问题。但降低剂量的同时,又将出现一个药效问题。而我们就可以用相同的LNP去做到更高的蛋白表达。从数据看,科镁信独有的生产工艺可提高MC3 LNP和ALC-0315 LNP的体内药效,在药效和耐受性之间取得一个平衡。
2. 第二个优势就是我们通过自主工艺的开发,做出了稳定的LNP,同时我们发现在老鼠体上还具有更高的蛋白表达效率。数据证明,得到的稳定PEG-free ALC-0315 LNP有更高的体内药效。因为我们知道LNP和mRNA药物通常是需要重复给药的,那人体内的anti-PEG抗体会识别并清除所有LNP。在我们以往的研发过程中,发现LNP给药次数越多,药效就会降低。那如果我们做出一个稳定的PEG-free的LNP,就能从根源上去解决这个问题。
3. 第三个优势是我们通过工艺开发方式,通过增加LNP表面修饰,达到主动靶向性。到目前为止,LNP都是被动的靶向。解决这个问题办法就是增加LNP表面的修饰。主要一个难点就是怎么将靶头接到LNP的表面。因为我们知道LNP是利用正电和负电的相互吸引,来形成一个自组装的结构。如果我们把一个富集电荷的结构(如多肽),接到LNP表面上的话,会极大地影响LNP的稳定性,不能够稳定存在,就不能工艺放大。
然后另外一点是,我们知道很多这种带有主动靶向性的靶头、带有功能性的靶头,通常都是带正电的。在我们传统的工艺下,这些带正电的靶头会倾向于和带负电荷的核酸结合成complex,而不是按照我们设计主动的去待在LNP的表面。所以说这个LNP的表面修饰是比较难做到的一个事情。那目前我们也是通过一些工艺的优化,做出多肽修饰的LNP。我们发现没有修饰的LNP,它在脾脏上面是没有任何的表达。然后我们修饰之后,我们可以看到脾脏的蛋白表达有极大的提高。实验表明,表面修饰的LNP表现出主动靶向性。
最后张翼博士总结了科镁信阳离子脂质高通量筛选平台的三个驱动引擎:
每月能生产~1g mRNA以支持体内筛选实验。工艺开发至百克级别 mRNA生产,以支持管线开发。单通道混合生产达20g LNP。
每周300只小鼠协助体内筛选。并且具有超10种不同给药方式进行定制化筛选。
每月测试1-2个新的脂质家族 ;每月合成200个高纯度科镁信专利结构脂质;每月合成~1000个LNP。我们相信在这三个引擎的推动下,科镁信今后能更好地去迭代阳离子脂质,然后找出适合我们临床应用的阳离子脂质。
LNP是核酸类药物的核心和价值所在。但阳离子脂质结构设计鲜有指导原则、体内筛选实验低通量和高成本、以及缺乏针对不同核酸载荷/给药方式的定制化开发这个三方面制约了LNP的发展。基于制约因素,科镁信LNP团队设计新型脂质骨架结构,建立高通量LNP筛选平台,开发最优制剂工艺,实现获得更高递送效率、更好耐受性的肝靶向LNP,以及具有高效肝外靶向的LNP的目标。
