



9月14日,江苏亚尧生物科技有限公司(以下简称“江苏亚尧”)自主研发的1类创新药ATR激酶抑制剂YY2201片收到美国FDA IND临床批件(IND173030),适应症针对晚期实体瘤。

图片来源:FDA批件
上海美迪西生物医药股份有限公司(以下简称“美迪西”)作为江苏亚尧的合作伙伴,为YY2201片的研发提供了药学研究(包括原料药和制剂)、临床前研究(包括药代动力学、安全性评价),以及IND注册申报等一站式研发服务,全力保障其高效、高质研发。
ATR激酶抑制剂YY2201片
剑指晚期实体瘤
YY2201片是由江苏亚尧自主开发的口服ATR小分子抑制剂,为类白色至淡黄色圆形薄膜衣片,除去包衣后显黄色。在已完成的系列非临床药理学研究、毒理学研究和药代动力学研究中,YY2201片展现出良好的体内、外活性、药代动力学特征及安全性,有望解决肿瘤患者未被满足的临床需求。
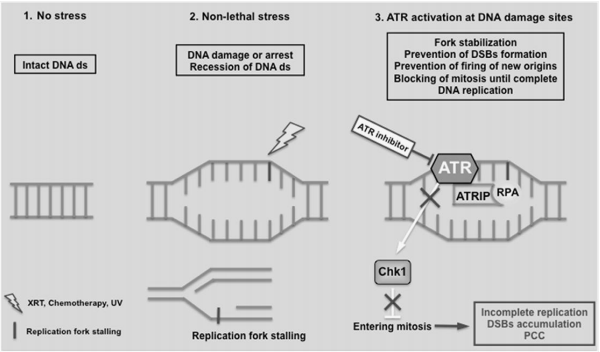
ATR,即共济失调毛细血管扩张突变基因和Rad3相关蛋白,是一种DNA修复的关键激酶,其在DNA损伤发生之后激活下游信号调控通路,阻滞肿瘤细胞周期并修复同源配对DNA,令肿瘤细胞凋亡调控功能失活。基因组不稳定性和突变性是肿瘤细胞发生发展的重要机制,靶向DNA修复相关激酶可以导致肿瘤细胞“合成致死”现象,因此ATR激酶抑制剂在癌症治疗上具有重要应用前景。此外,ATR对细胞的生长增殖等过程同样至关重要。有研究表明ATR双等位基因的丧失会导致早期胚胎致死。ATR抑制剂的主要作用是抑制S期和G2/M细胞周期检查点导致复制应激叉(RS)增加并过早进入有丝分裂期导致危象,诱发S期和G2期DNA发生同源重组修复(HRR)和DNA双链断裂(DSB)。因此,ATR的选择性抑制为肿瘤治疗提供了新的思路,也为肿瘤研究提供了新的工具。当前,尽管ATR抑制剂在全球市场尚未有产品正式获批上市,但这一领域的研发正以前所未有的速度推进,预示着其在未来肿瘤治疗中的巨大潜力。
江苏亚尧YY2201片新药获FDA IND批件,这一里程碑式的成就不仅彰显了江苏亚尧在肿瘤研发领域的深厚实力,更是对其创新能力的高度认可。
一站式临床前研发服务平台
美迪西赋能药物研发“多快好省”
在新药研发的激烈竞争中,速度和品质至关重要。美迪西,作为临床前研发领域的资深耕耘者,二十载深耕不辍,凭借对行业需求的敏锐洞察与不断拓展,成功构建了“一站式生物医药临床前研发服务平台”。该平台无缝衔接了从药物发现、药学研究到临床前研究的每一个关键环节,形成了一条高效流畅的研发链路,为新药快速获批临床提供了有力保障。
值得关注的是,美迪西在肿瘤药物研发这一前沿阵地,已构建起一套全面而先进的药效评价体系,拥有440+种肿瘤药效模型(包括118种PD原位模型、同种肿瘤移植模型、异种肿瘤移植模型、人源化肿瘤移植模型等),累积了深厚的研发实力与经验,持续推动肿瘤药物的创新研发。美迪西祝贺江苏亚尧YY2201片获批FDA临床,并期待该药物在临床试验中取得积极结果,早日为晚期肿瘤患者带来福音。同时美迪西将持续专注于一站式生物医药研发服务平台的创新与发展,为全球药物研发提供更高质量、更快速的服务支持。
关于江苏亚尧
追求卓越、精益求精、和谐发展、不断创新!江苏亚尧生物科技有限公司由多位海归科学家与国内的医学、药学专家共同创建,位于江苏南京江北新区药谷,是一家综合性的医药研发、制造公司。2019年完成初期融资,2020年被南京江北新区作为重点项目引入药谷。
公司具备完善的组织机构和质量管理体系、建立了较为完整的文件系统,能有效地对药品全生命周期进行质量把控;公司于2022年06月25日获得江苏省药品监督管理局核发的《药品生产许可证》。公司具有持续开发能力,公司携已开发的研究成果,联合资本的支持,已成为国家科技型中小企业,申请国家高新技术企业。公司致力于靶向药物的开发研究,目前多个创新药物在研,现拥有中国、美国、欧盟及日本等国家的专利授权。2024年下半年将开展第一个创新药Ⅰ期临床研究,预期近两年开展不少于两个Ⅰ期,一个Ⅱ期药物临床研究。
公司目前已申请发明专利3项,获得中、美、日、欧洲授权5项。其中一项发明专利已成功申请中国大陆、台湾地区,并通过PCT国际申请成功进入欧、美、日、韩、加、澳、巴西、印度等国家与地区。
 相关新闻
相关新闻